2025/06/23 17:55
ISHA 2025へようこそ!
研究成果の概要
超高齢化社会を迎えた現在、認知症の早期診断や治療法の開発は、早急に解決するべき課題です。アルツハイマー病は、認知症の原因疾患の大部分を占めており、ひとたび発症すると進行性に悪化する難病として、多くの患者やその家族を苦しめています。アルツハイマー病の原因は、脳にアミロイドβが蓄積することに起因すると考えられています(アミロイド仮説)。近年の分子生物学的手法を用いた基礎的研究の進歩により、根本的な治療法として病態に基づいた分子標的治療法(アミロイド抗体医薬)が特定の臨床現場では使用可能になっています。しかし、現状では十分な治療効果を挙げているとは言い難い状況です。根本的な治療法の開発が困難である理由として、次のような要因が考えられます。1)認知症の発症時にはすでに病態が進行しており、分子標的治療法による抑止効果が発揮できないこと、2)疾患の進行を抑制するという薬効を評価するための客観的指標が確立されていないこと。これらはいずれも、早期診断の方法、あるいは、抑止効果を正確に評価できるバイオマーカーの確立が根本的な治療法の開発には欠かすことができないことを示しています。
血液脳関門は、脳を保護するために生来人類に備わっているバリアー機構です。身体中に張り巡らされている体循環系の毛細血管は有窓性であり、組織との必要な物質交換が円滑に行われています。一方で、中枢神経系の毛細血管は血液脳関門の存在により無窓性の構造をとります。この血液脳関門の機能的な役割は、① 有害物質の中枢神経系への流入制限、② 必須物質の選択的な取り込み、③ 有害物質の排出の大きく三つに分けられます。病理組織学的研究や動物実験により、アルツハイマー病の脳にはアミロイドβやリン酸化タウ蛋白、鉄などの不要な物質が蓄積していること、また、これらの排せつを担う血液脳関門が機能障害を起こしていることがわかっています。しかし、アルツハイマー病患者と血液脳関門機能障害との直接的な関連性は、これまで明らかにされていませんでした。
名古屋市立大学大学院医学研究科の松川則之教授、打田佑人研究員(神経内科学)らの研究チームは、ヒトの血液脳関門機能を可視化する画像技術の開発を目指して、これまでに磁気共鳴画像(Magnetic Resonance Image:MRI)を応用した臨床画像研究を行ってきました。この度、名古屋市総合リハビリテーションセンターの堀本佳彦部長らの研究チームと共同して、早期アルツハイマー病患者を対象に最新技術を駆使したMRIや陽電子放出断層撮影(Positron Emission Tomography:PET)を用いた多施設共同臨床研究を行いました。本研究により新たに発見された知見として、i) 早期アルツハイマー病患者において血液脳関門機能障害を来している部位が生体脳で可視化できること、ii) 血液脳関門機能障害を来している部位がアミロイドβや鉄の蓄積と関連していること、iii) 血液脳関門機能障害により部位特異的な認知機能に悪影響を及ぼしていることを、世界で初めて明らかにし、英国科学誌「Journal of Neurology, Neurosurgery, and Psychiatry」に報告しました。
本研究の特色は、早期アルツハイマー病患者をアポリポ蛋白Eで層別化したことにあります。アポリポ蛋白Eは、19番染色体上にあるAPOE遺伝子によって決まる三つのタイプ(ɛ2、ɛ3、ɛ4)があり、ɛ4はアルツハイマー病のリスク因子であることが確立しています。より具体的には、ɛ4を1つ有する場合(ヘテロ接合体)は3-4倍、二つ有する場合(ホモ接合体)は9-15倍の発症リスクであることが知られています。私たちは、ɛ4を有するアルツハイマー病の脳では、血液脳関門機能障害のために有害な物質の排出が円滑に行われず、アミロイドβや鉄が蓄積するという仮説を立て、検証しました。本研究により、血液脳関門機能障害部位を非侵襲的なMRIを用いて可視化できたことは、アルツハイマー病の疾患バイオマーカーとして早期診断や治療法の開発に役立つ重要な発見です。今後、この方法を応用して、アルツハイマー病の根本的な制圧に向けたさらなる研究が期待されます。
ポイント
・ アルツハイマー病は認知症の原因疾患として最も多く、早期診断や治療法の開発が望まれます。
・ 血液脳関門は、脳を保護する中枢神経組織特有のバリアー機構です。
・ 血液脳関門の機能障害は、アルツハイマー病の発症や進行に関わっています。
・ 血液脳関門機能の評価方法は確立されておらず、客観的なモニタリングを可能とする画像バイオ
マーカーの開発が求められています。
・ 本研究では、早期アルツハイマー病を対象に、最新の画像技術を用いて血液脳関門の機能障害と
その部位の特定に成功しました。
・ 早期アルツハイマー病の中でも、特にAPOE ɛ4を有している患者において血液脳関門の機能障
害が顕著に認められました。
・ 本研究の成果により、血液脳関門機能の可視化が可能になり、血液脳関門の機能維持に根ざした
治療・予防法の開発が期待されます。
掲載された論文の要旨
【背景】
血液脳関門が機能障害に陥ると、脳の有害物質の排せつに支障を生じます。本研究では、APOE ɛ4で層別化した早期アルツハイマー病患者を対象にして、最新の画像技術を用いて解剖学的部位毎の血液脳関門機能を測定し、アミロイドβや鉄沈着、部位特異的な認知機能との相関を調べました。
【方法】
はじめに、ɛ4を有さない患者24人(ɛ3/ɛ3)、ɛ4を1つ有するヘテロ接合患者22人(ɛ3/ɛ4)、ɛ4を2つ有するホモ接合患者20人(ɛ4/ɛ4)の患者属性や身体学的検査、神経学的検査、高次脳機能検査を記録しました。続いて、画像検査に同意された患者を対象に、脳MRIおよびPET検査を施行しました。脳MRIでは、まず頸(けい)動脈領域にラジオ波を照射して血管内の水分子を磁気的に標識(① Labeling pulse:図1)します。ラベリングされた水分子は、脳内の毛細血管に到達すると組織の間質液に向かって拡散を始めます。血管内の水分子と組織の拡散係数は大きく異なるため、適切な拡散強調パルスを照射することで(② Motion probing gradient pulse)、血液脳関門を介した水クリアランス [blood–brain barrier (BBB) kw index] を測定することが可能です。本手法は、Diffusion-prepared arterial spin labeling (DP-ASL) と呼称され、撮像時間は約15分間です。従来のDynamic contrast-enhanced MRIではガドリニウム造影剤の使用が必須でしたが、本手法ではラベリングパルスを用いているため、非造影単純MRI(3-Tesla機器)で撮像が可能です。
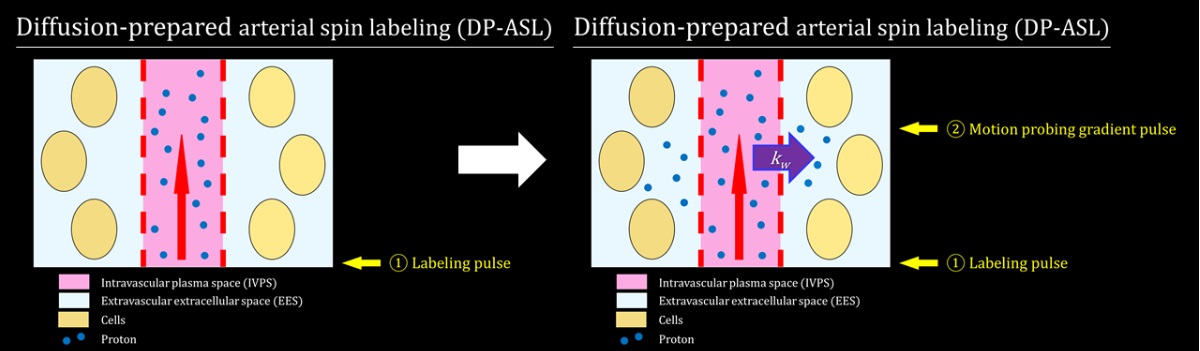
図1 Diffusion-prepared arterial spin labeling(DP-ASL)の撮像原理
DP-ASLに続いて、定量的磁化率画像(Quantitative susceptibility mapping:QSM)を用いた鉄沈着量、PiB-PETを用いたアミロイドβ沈着量を、各患者における脳解剖学的部位毎に測定しました(図2)。測定対象の脳解剖学的部位としては、まず、Thal amyloid phaseに従って全脳領域を概観しました。その後、アルツハイマー病において病理組織学的に重要な部位である前頭葉や内側・外側側頭葉、頭頂葉、楔前部、後部帯状回に絞って、各群間の画像定量値 [BBB kw index、QSM value、standard uptake value ratio (SUVR)]を比較しました。最後に、部位特異的な認知機能との相関を探索的に解析しました。
図2 BBB kw map、QSM、Amyloid-PETの代表的画像
【結果】
APOE ɛ4を多く有するほど、BBB kw indexが低下しており、鉄やアミロイドβの沈着量が増加していることが明らかになりました。特に、Thal amyloid phase 1 とThal amyloid phase 2において、各画像定量値に有意な差が認められました(図3)。疾患特異的部位における仮説検証的な群間解析においては、前頭葉 [ɛ3/ɛ3 vs ɛ3/ɛ4 vs ɛ4/ɛ4 = BBB kw index (min-1): 110.29 ± 8.77 vs 94.11 ± 8.34 vs 77.95 ± 6.86, QSM value (×10-3 ppm): −3.93 ± 0.61 vs −3.12 ± 0.63 vs −1.04 ± 0.68, SUVR of Amyloid-PET: 1.62 ± 0.13 vs 1.98 ± 0.14 vs 2.16 ± 0.16] と内側側頭葉 [ɛ3/ɛ3 vs ɛ3/ɛ4 vs ɛ4/ɛ4 = BBB kw index (min-1): 93.58 ± 7.81 vs 86.73 ± 8.12 vs 76.08 ± 6.95, QSM value (×10-3 ppm): −3.26 ± 0.69 vs −1.38 ± 0.71 vs −0.64 ± 0.72, SUVR of Amyloid-PET: 1.45 ± 0.12 vs 1.67 ± 0.12 vs 1.79 ± 0.14] で各画像定量値に明瞭な差が認められました。認知機能は、前頭葉機能を反映するTrail Making Test B timesと内側側頭葉機能を反映するLogical Memory II scoresにおいて、それぞれBBB kw indexと負の相関 (r = −0.435, 95% CI −0.613 to −0.216)、正の相関 (r = 0.423, 95% CI 0.202 to 0.603)を示しました(図4)。
図3 Thal amyloid phase毎の定量値 図4 BBB kw indexと認知機能との相関解析結果
【結論】
APOE ɛ4を有する早期アルツハイマー病患者では、血液脳関門を介した水クリアランス機能障害に伴って、鉄やアミロイドβの沈着量が増加していることが明らかになりました。
【研究の意義と今後の展開】
本多施設共同臨床画像研究では、APOE ɛ4の有無で層別化した早期アルツハイマー病患者を対象として、最新の画像技術を駆使して血液脳関門の機能障害とその部位の特定に成功しました。本研究成果により、これまでは難しかったヒト生体脳における血液液脳関門の機能評価が可能になり、血液脳関門の機能維持に根ざした治療・予防法の開発が期待されます。
【研究助成】
本研究は、第24回日本医学会総会記念医学振興基金と興和生命科学振興財団からの助成を受けて遂行されました。
【論文タイトル】
APOE ɛ4 dose associates with increased brain iron and β-amyloid via blood–brain
barrier dysfunction
【著者】
打田佑人1, 2、菅博人3、櫻井圭太4、堀本佳彦5、林絵美6、飯田昭彦6、岡村信行7、大石健一8、
松川則之1* (*Corresponding author)
(以下、論文投稿時の所属機関)
1. 名古屋市立大学大学院医学研究科神経内科学
2. 豊川市民病院脳神経内科
3. 名古屋大学大学院医学系研究科総合保健学専攻
4. 国立長寿医療研究センター放射線診療部
5. 名古屋市総合リハビリテーションセンター脳神経内科
6. 名古屋市総合リハビリテーションセンター放射線科
7. 東北医科薬科大学医学部薬理学
8. ジョンズホプキンス大学放射線科
【掲載学術誌】
学術誌名:Journal of Neurology, Neurosurgery, and Psychiatry
DOI番号:10.1136/jnnp-2021-328519
【研究に関する問い合わせ】
名古屋市立大学大学院医学研究科神経内科学 教授 松川則之
名古屋市瑞穂区瑞穂町字川澄 1
TEL:052-853-8094 FAX:052-852-3590
E-mail:norim@med.nagoya-cu.ac.jp
【報道に関する問い合わせ】
名古屋市立大学 医学・病院管理部経営課
名古屋市瑞穂区瑞穂町字川澄1
TEL:052-858-7114 FAX:052-858-7537
E-mail:hpkouhou@sec.nagoya-cu.ac.jp
(2022/06/02 11:07)
2025/06/23 17:55
ISHA 2025へようこそ!
2025/06/20 16:45
「アウティング」が性的マイノリティのメンタルヘルス悪化に関連することを解明
~性的マイノリティの9.3%が「アウティング」を経験~
2025/06/06 12:24
第14回日本認知症予防学会学術集会