“見た目はそっくり、中身は違う”(C-グリコシド型)擬複合糖質を開発
国立研究開発法人医薬基盤・健康・栄養研究所
分岐合成法の確立と生物活性が大きく異なる多様なアナログ群の創出
1.天然に存在する糖鎖・複合糖質の構造を模倣するC-グリコシドアナログは、糖加水分解酵素に分解されない有用な生物機能分子として期待されていますが、その生物化学的研究は遅れていました。 2.今回、C-グリコシド炭素上(糖連結部位)に水素またはフッ素原子を持つ3種のアナログ分子を触媒的・立体選択的に分岐合成する手法を確立し、その独特の生物活性を見出しました。 3.今後、この合成手法に代表される「連結部位編集戦略(Linkage-Editing Strategy)」により、糖鎖・複合糖質を活用したユニークな生物活性分子(免疫機能を制御できる創薬シーズなど)の創出が期待されます。

天然型糖鎖・複合糖質の構造をわずかに改変したアナログ分子(擬糖鎖・擬複合糖質)の開発は、創薬研究において極めて重要ですが、合成の煩雑さなどの理由から、限られた検討にとどまっていました。
九州大学大学院薬学研究院の平井剛教授を中心とする研究グループ(摂南大学農学部 加藤直樹准教授、医薬基盤・健康・栄養研究所 國澤純センター長ら、大阪大学微生物病研究所 山崎晶教授ら、理化学研究所環境資源科学研究センター 越野広雪ユニットリーダー 高橋俊二ユニットリーダー、九州大学先導物質化学研究所 友岡克彦教授ら)は、糖加水分解酵素により分解されないC-グリコシド型複合糖質の新規多様化戦略を考案し、光エネルギーと触媒反応を駆使して効率的な分岐合成法を開発しました。本手法では3種の連結部位(CH2, (R)-CHF, (S)-CHF型)を持つC-グリコシドアナログの分岐合成が可能になり、実際に擬イソマルトースおよび擬α-ガラクトシルセラミドの合成に成功しました。さらに合成したCH2-イソマルトースは天然型と比較して極めて高いアミラーゼ誘導活性を示し、(R)-CHF-α-ガラクトシルセラミドは天然型とは真逆のインバリアントナチュラルキラーT (iNKT)細胞のアンタゴニスト様活性を示すことを明らかにしました。
本研究成果は、アメリカ化学会が出版する国際誌「Journal of American Chemical Society」のオンライン版にて2024年1月9日(現地時間)に掲載されました。
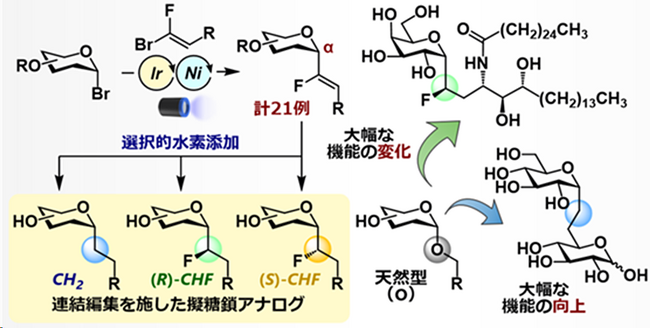
本研究の概要図
【研究の背景と経緯】
第3の生命鎖と呼ばれる糖鎖・複合糖質は、分子認識や免疫反応に重要な役割を担っているため、創薬・生物学分野においてその機能解明が求められています。しかし、糖鎖・複合糖質はグリコシド結合を介して他の分子と結びついており、この結合は特定の酵素により切断されてしまいます。一方、天然の糖鎖・複合糖質のグリコシド結合の酸素原子を炭素に置換したC-グリコシドアナログは、糖鎖の構造を模倣しながらも、糖加水分解酵素によって分解されません。このため、C-グリコシドアナログは糖鎖の機能解明に有用なツールであると考えられていますが、合成が煩雑であるため、その機能を検証する研究が遅れていました。
今回共同研究グループは、C-グリコシドアナログの構造を多様化する新たな戦略として、連結部位編集戦略を考案しました。これは、C-グリコシド炭素上の水素原子を小さい官能基で置換することで、新たなアナログ分子を創出する戦略です。C-グリコシド炭素上にフッ素原子を導入すると、特有の立体電子効果によりグリコシド結合の回転(φ角)が制御されます(図1)。一方、フッ素を持たないCH2-連結型は、立体電子効果が効かないためφ角が柔軟に回転します。それぞれ固有の特性をもつCH2-、(R)-CHF-、(S)-CHF-連結型アナログを、共通の中間体から網羅的に分岐合成する効率的手法は存在しませんでした。この効率的な分岐合成法を開発すれば、分子設計概念の実証と創薬およびケミカルバイオロジー研究の加速に大きく貢献すると期待しました。
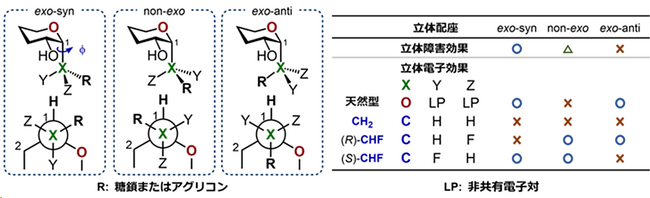
図1. 天然型、CH2-、(R)-CHF-、(S)-CHF-グリコシドの配座特性の違い:天然型O-グリコシドは、立体電子効果(エキソアノマー効果)と立体障害によりexo-syn配座を優先的に取ることが報告されています。一方、置換基を持たないCH2-グリコシドは、立体電子効果による配座制御効果がないため柔軟な配座を有しています。フッ素原子を導入した(R)-および(S)-CHF-グリコシドは、天然型とは別の立体電子効果(ゴーシュ効果)により配座が制御され、O-やCH2-グリコシドとは異なる配座特性を有すると考えられます。
【研究の内容と成果】
本研究ではまず、C-グリコシドアナログの共通中間体となるフルオロビニル-C-グリコシドの合成法と、3種のC-グリコシドアナログの分岐合成法を開発しました(図2,3)。各段階で鍵となるのは、立体および化学選択性です。糖と糖またはアグリコンをC-C結合で連結するC-グリコシル化反応は、幅広い組み合わせの糖・アグリコンへの適用が期待されますが、技術課題として片方の異性体を選択的に与える方法を開発する必要がありました(図2)。2,3位がカーボネートで保護された糖供与体とBrFオレフィンを、光触媒、ニッケル触媒存在下、青色LEDを照射すると、高いα選択性と収率でフルオロビニル-C-グリコシドを合成できました。糖供与体を2,3-カーボネート保護することで配座が固定され、グリコシルラジカルを立体電子効果的に有利なα面に配向することが、α選択性のコントロールに重要でした。本反応によって、糖や脂質を含む合計21例のアグリコンに適用できることを実証し、広範な擬複合糖質合成に展開できる手法の開発に成功しました。
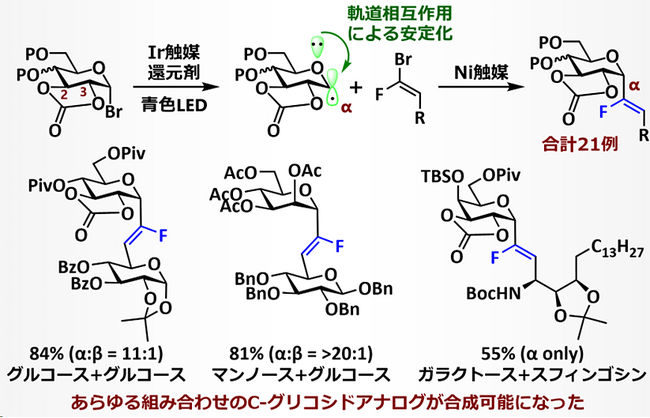
図2. 光酸化還元カップリング反応によるフルオロビニル-C-グリコシル化反応:光エネルギーを利用した温和な反応条件により、広範なブロモ糖とBrFオレフィンを直接連結できるようになりました。糖供与体には、様々な保護パターンを有するグルコース、ガラクトース、マンノースの計8種、糖や脂質から2工程で合成できるBrFオレフィンの計13種が利用可能であることを示しました。
合成したフルオロビニル-C-グリコシドからのCH2-、(R)-CHF-、(S)-CHF-グリコシドの分岐合成は、触媒制御により達成できると考えました(図3)。触媒を徹底的に検討した結果、白金炭素触媒やロジウムアルミナ触媒はCH2グリコシドを、水酸化パラジウム触媒は(S)-CHF-グリコシドを、Crabtree触媒は(R)-CHF-グリコシドを与えることを見出しました。開発した手法によって、それぞれ3種ずつの炭素連結型イソマルトースおよびα-ガラクトシルセラミドの合成を達成しました。
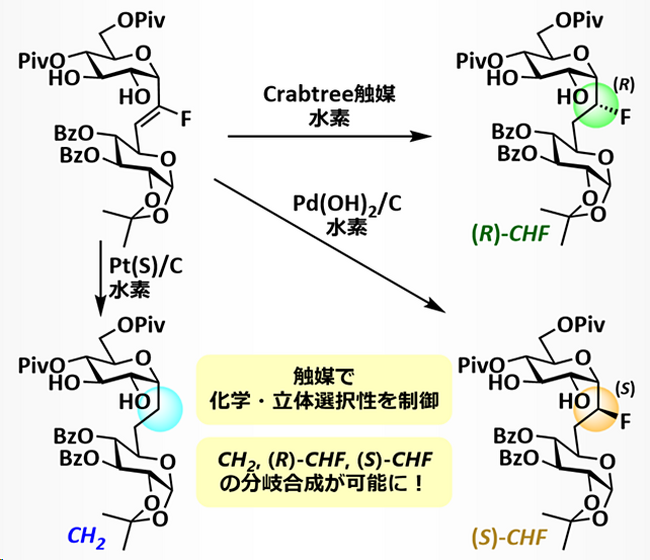
図3. 触媒制御による化学および立体選択的な水素添加反応:フルオロビニル-C-グリコシドの水素添加反応では、白金系の水素添加触媒を用いるとフッ素が除去されたCH2-グリコシドを与える傾向があることがわかりました。一方、水酸化パラジウム触媒(Pearlman触媒)では、立体的に空いた面から水素添加が進行することで(S)-CHF-グリコシドを与え、Crabtree触媒はヒドロキシ基の配向効果により(R)-CHFグリコシドを構築できました。
連結部位編集戦略の概念実証のため、合成した炭素連結型イソマルトースおよびα-ガラクトシルセラミドの生物活性を評価しました(図4)。天然型イソマルトースは糸状菌Aspergillus nidulansのアミラーゼ生産を誘導する活性があることが知られています。これに対しCH2連結型イソマルトースは、天然型よりも大幅に高いアミラーゼ生産誘導活性を示すことが明らかになりました。天然型α-ガラクトシルセラミドは、マウス樹状細胞上のCD1dに提示され、T細胞受容体を介してiNKT細胞を活性化することが知られています。一方、(R)-CHF連結型α-ガラクトシルセラミドはCD1dへの提示は示唆されたものの、iNKT細胞を逆に活性化せず、むしろ不活性化することを見出しました。これらの結果より、連結部位編集戦略が多様な生物活性を有する擬複合糖質の創出に有効な戦略であることを実証しました。
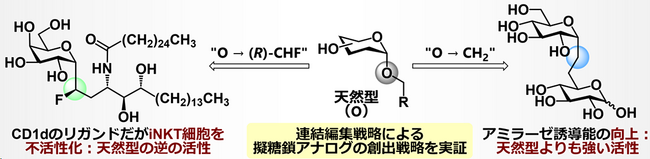
図4. C-グリコシドアナログの生物活性評価:いずれのアナログも、天然型と3種の炭素連結型アナログの活性を比較したところ、興味深い生物活性の変化を見出しました。連結部位編集戦略により配座特性が変化することや、受容体タンパク質との相互作用が変化することが、生物活性変化をもたらすと考えています。
【今後の展開】
本研究により、従来合成が煩雑であったCH2-およびCHF-グリコシドアナログの網羅的な合成が可能となりました。今後、連結部位編集戦略を基盤として様々な擬複合糖質を創生することで、創薬研究およびケミカルバイオロジー研究の発展につながると期待できます。
【用語の説明】
糖鎖 :複数の糖がグリコシド結合により、鎖のように連なった化合物。細胞内のタンパク質などと相互作用し、免疫反応等の制御に関与する。
糖加水分解酵素:糖のグリコシド結合に作用し、加水分解する酵素の総称。
アナログ分子 :元の分子の構造や性質が類似しているが、異なる組成を持つ別の分子。
アグリコン :配糖体を構成する糖以外の成分。配糖体を加水分解することで得られる。
立体電子効果 :主に結合を構成する元素の電子的特性によって、分子の立体配座に影響を与える現象のこと。
光触媒 :光エネルギーにより活性化(励起)され、酸化・還元作用を示す触媒。
アミラーゼ :でんぷんなどを分解する糖加水分解酵素の一種で、ヒトでは食物の消化を助ける働きをもつ。
樹状細胞 :免疫細胞の一種で、異物の情報を他の免疫細胞に伝えたり、食作用により異物を排除したりする機能をもつ。
CD1d :樹状細胞のような抗原提示細胞上に存在する抗原タンパク質。α-ガラクトシルセラミ
ドはマウスCD1dに提示され、インバリアントナチュラルキラーT(iNKT)細胞上のT細胞受容体に認識されることでiNKT細胞を活性化する。
【謝辞】
本研究成果は、学術変革領域研究(A)「炭素資源変換を革新するグリーン触媒化学」(研究総括:大井 貴史、23H04913)、および国立研究開発法人日本医療研究開発機構(AMED)の先進的研究開発戦略センター(SCARDA)事業における、ワクチン・新規モダリティ研究開発事業『革新的アジュバント・ワクチンキャリアの開発と技術支援ならびにデータベースの構築』の一環として得られました。また本研究は、上記に加え、科学研究費補助金(基盤研究(B)、挑戦的研究、若手研究)、LeaP科学財団の支援を受けて実施したものです。
【論文情報】
掲載誌:Journal of American Chemical Society
タイトル:Linkage-Editing pseudo-Glycans: A Reductive α-Fluorovinyl-C-Glycosylation Strategy to Create Glycan Analogs with Altered Biological Activities
著者名:Takahiro Moriyama, Makoto Yoritate, Naoki Kato, Azusa Saika, Wakana Kusuhara, Shunsuke Ono, Takahiro Nagatake, Hiroyuki Koshino, Noriaki Kiya, Natsuho Moritsuka, Riko Tanabe, Yu Hidaka, Kazuteru Usui, Suzuka Chiba, Noyuri Kudo, Rintaro Nakahashi, Kazunobu Igawa, Hiroaki Matoba, Katsuhiko Tomooka, Eri Ishikawa, Shunji Takahashi, Jun Kunisawa, Sho Yamasaki, and Go Hirai
D O I:10.1021/jacs.3c12581

企業プレスリリース詳細へ
PR TIMESトップへ
分岐合成法の確立と生物活性が大きく異なる多様なアナログ群の創出
1.天然に存在する糖鎖・複合糖質の構造を模倣するC-グリコシドアナログは、糖加水分解酵素に分解されない有用な生物機能分子として期待されていますが、その生物化学的研究は遅れていました。 2.今回、C-グリコシド炭素上(糖連結部位)に水素またはフッ素原子を持つ3種のアナログ分子を触媒的・立体選択的に分岐合成する手法を確立し、その独特の生物活性を見出しました。 3.今後、この合成手法に代表される「連結部位編集戦略(Linkage-Editing Strategy)」により、糖鎖・複合糖質を活用したユニークな生物活性分子(免疫機能を制御できる創薬シーズなど)の創出が期待されます。

天然型糖鎖・複合糖質の構造をわずかに改変したアナログ分子(擬糖鎖・擬複合糖質)の開発は、創薬研究において極めて重要ですが、合成の煩雑さなどの理由から、限られた検討にとどまっていました。
九州大学大学院薬学研究院の平井剛教授を中心とする研究グループ(摂南大学農学部 加藤直樹准教授、医薬基盤・健康・栄養研究所 國澤純センター長ら、大阪大学微生物病研究所 山崎晶教授ら、理化学研究所環境資源科学研究センター 越野広雪ユニットリーダー 高橋俊二ユニットリーダー、九州大学先導物質化学研究所 友岡克彦教授ら)は、糖加水分解酵素により分解されないC-グリコシド型複合糖質の新規多様化戦略を考案し、光エネルギーと触媒反応を駆使して効率的な分岐合成法を開発しました。本手法では3種の連結部位(CH2, (R)-CHF, (S)-CHF型)を持つC-グリコシドアナログの分岐合成が可能になり、実際に擬イソマルトースおよび擬α-ガラクトシルセラミドの合成に成功しました。さらに合成したCH2-イソマルトースは天然型と比較して極めて高いアミラーゼ誘導活性を示し、(R)-CHF-α-ガラクトシルセラミドは天然型とは真逆のインバリアントナチュラルキラーT (iNKT)細胞のアンタゴニスト様活性を示すことを明らかにしました。
本研究成果は、アメリカ化学会が出版する国際誌「Journal of American Chemical Society」のオンライン版にて2024年1月9日(現地時間)に掲載されました。
本研究の概要図

【研究の背景と経緯】
第3の生命鎖と呼ばれる糖鎖・複合糖質は、分子認識や免疫反応に重要な役割を担っているため、創薬・生物学分野においてその機能解明が求められています。しかし、糖鎖・複合糖質はグリコシド結合を介して他の分子と結びついており、この結合は特定の酵素により切断されてしまいます。一方、天然の糖鎖・複合糖質のグリコシド結合の酸素原子を炭素に置換したC-グリコシドアナログは、糖鎖の構造を模倣しながらも、糖加水分解酵素によって分解されません。このため、C-グリコシドアナログは糖鎖の機能解明に有用なツールであると考えられていますが、合成が煩雑であるため、その機能を検証する研究が遅れていました。
今回共同研究グループは、C-グリコシドアナログの構造を多様化する新たな戦略として、連結部位編集戦略を考案しました。これは、C-グリコシド炭素上の水素原子を小さい官能基で置換することで、新たなアナログ分子を創出する戦略です。C-グリコシド炭素上にフッ素原子を導入すると、特有の立体電子効果によりグリコシド結合の回転(φ角)が制御されます(図1)。一方、フッ素を持たないCH2-連結型は、立体電子効果が効かないためφ角が柔軟に回転します。それぞれ固有の特性をもつCH2-、(R)-CHF-、(S)-CHF-連結型アナログを、共通の中間体から網羅的に分岐合成する効率的手法は存在しませんでした。この効率的な分岐合成法を開発すれば、分子設計概念の実証と創薬およびケミカルバイオロジー研究の加速に大きく貢献すると期待しました。

図1. 天然型、CH2-、(R)-CHF-、(S)-CHF-グリコシドの配座特性の違い:天然型O-グリコシドは、立体電子効果(エキソアノマー効果)と立体障害によりexo-syn配座を優先的に取ることが報告されています。一方、置換基を持たないCH2-グリコシドは、立体電子効果による配座制御効果がないため柔軟な配座を有しています。フッ素原子を導入した(R)-および(S)-CHF-グリコシドは、天然型とは別の立体電子効果(ゴーシュ効果)により配座が制御され、O-やCH2-グリコシドとは異なる配座特性を有すると考えられます。
【研究の内容と成果】
本研究ではまず、C-グリコシドアナログの共通中間体となるフルオロビニル-C-グリコシドの合成法と、3種のC-グリコシドアナログの分岐合成法を開発しました(図2,3)。各段階で鍵となるのは、立体および化学選択性です。糖と糖またはアグリコンをC-C結合で連結するC-グリコシル化反応は、幅広い組み合わせの糖・アグリコンへの適用が期待されますが、技術課題として片方の異性体を選択的に与える方法を開発する必要がありました(図2)。2,3位がカーボネートで保護された糖供与体とBrFオレフィンを、光触媒、ニッケル触媒存在下、青色LEDを照射すると、高いα選択性と収率でフルオロビニル-C-グリコシドを合成できました。糖供与体を2,3-カーボネート保護することで配座が固定され、グリコシルラジカルを立体電子効果的に有利なα面に配向することが、α選択性のコントロールに重要でした。本反応によって、糖や脂質を含む合計21例のアグリコンに適用できることを実証し、広範な擬複合糖質合成に展開できる手法の開発に成功しました。

図2. 光酸化還元カップリング反応によるフルオロビニル-C-グリコシル化反応:光エネルギーを利用した温和な反応条件により、広範なブロモ糖とBrFオレフィンを直接連結できるようになりました。糖供与体には、様々な保護パターンを有するグルコース、ガラクトース、マンノースの計8種、糖や脂質から2工程で合成できるBrFオレフィンの計13種が利用可能であることを示しました。
合成したフルオロビニル-C-グリコシドからのCH2-、(R)-CHF-、(S)-CHF-グリコシドの分岐合成は、触媒制御により達成できると考えました(図3)。触媒を徹底的に検討した結果、白金炭素触媒やロジウムアルミナ触媒はCH2グリコシドを、水酸化パラジウム触媒は(S)-CHF-グリコシドを、Crabtree触媒は(R)-CHF-グリコシドを与えることを見出しました。開発した手法によって、それぞれ3種ずつの炭素連結型イソマルトースおよびα-ガラクトシルセラミドの合成を達成しました。

図3. 触媒制御による化学および立体選択的な水素添加反応:フルオロビニル-C-グリコシドの水素添加反応では、白金系の水素添加触媒を用いるとフッ素が除去されたCH2-グリコシドを与える傾向があることがわかりました。一方、水酸化パラジウム触媒(Pearlman触媒)では、立体的に空いた面から水素添加が進行することで(S)-CHF-グリコシドを与え、Crabtree触媒はヒドロキシ基の配向効果により(R)-CHFグリコシドを構築できました。
連結部位編集戦略の概念実証のため、合成した炭素連結型イソマルトースおよびα-ガラクトシルセラミドの生物活性を評価しました(図4)。天然型イソマルトースは糸状菌Aspergillus nidulansのアミラーゼ生産を誘導する活性があることが知られています。これに対しCH2連結型イソマルトースは、天然型よりも大幅に高いアミラーゼ生産誘導活性を示すことが明らかになりました。天然型α-ガラクトシルセラミドは、マウス樹状細胞上のCD1dに提示され、T細胞受容体を介してiNKT細胞を活性化することが知られています。一方、(R)-CHF連結型α-ガラクトシルセラミドはCD1dへの提示は示唆されたものの、iNKT細胞を逆に活性化せず、むしろ不活性化することを見出しました。これらの結果より、連結部位編集戦略が多様な生物活性を有する擬複合糖質の創出に有効な戦略であることを実証しました。

図4. C-グリコシドアナログの生物活性評価:いずれのアナログも、天然型と3種の炭素連結型アナログの活性を比較したところ、興味深い生物活性の変化を見出しました。連結部位編集戦略により配座特性が変化することや、受容体タンパク質との相互作用が変化することが、生物活性変化をもたらすと考えています。
【今後の展開】
本研究により、従来合成が煩雑であったCH2-およびCHF-グリコシドアナログの網羅的な合成が可能となりました。今後、連結部位編集戦略を基盤として様々な擬複合糖質を創生することで、創薬研究およびケミカルバイオロジー研究の発展につながると期待できます。
【用語の説明】
糖鎖 :複数の糖がグリコシド結合により、鎖のように連なった化合物。細胞内のタンパク質などと相互作用し、免疫反応等の制御に関与する。
糖加水分解酵素:糖のグリコシド結合に作用し、加水分解する酵素の総称。
アナログ分子 :元の分子の構造や性質が類似しているが、異なる組成を持つ別の分子。
アグリコン :配糖体を構成する糖以外の成分。配糖体を加水分解することで得られる。
立体電子効果 :主に結合を構成する元素の電子的特性によって、分子の立体配座に影響を与える現象のこと。
光触媒 :光エネルギーにより活性化(励起)され、酸化・還元作用を示す触媒。
アミラーゼ :でんぷんなどを分解する糖加水分解酵素の一種で、ヒトでは食物の消化を助ける働きをもつ。
樹状細胞 :免疫細胞の一種で、異物の情報を他の免疫細胞に伝えたり、食作用により異物を排除したりする機能をもつ。
CD1d :樹状細胞のような抗原提示細胞上に存在する抗原タンパク質。α-ガラクトシルセラミ
ドはマウスCD1dに提示され、インバリアントナチュラルキラーT(iNKT)細胞上のT細胞受容体に認識されることでiNKT細胞を活性化する。
【謝辞】
本研究成果は、学術変革領域研究(A)「炭素資源変換を革新するグリーン触媒化学」(研究総括:大井 貴史、23H04913)、および国立研究開発法人日本医療研究開発機構(AMED)の先進的研究開発戦略センター(SCARDA)事業における、ワクチン・新規モダリティ研究開発事業『革新的アジュバント・ワクチンキャリアの開発と技術支援ならびにデータベースの構築』の一環として得られました。また本研究は、上記に加え、科学研究費補助金(基盤研究(B)、挑戦的研究、若手研究)、LeaP科学財団の支援を受けて実施したものです。
【論文情報】
掲載誌:Journal of American Chemical Society
タイトル:Linkage-Editing pseudo-Glycans: A Reductive α-Fluorovinyl-C-Glycosylation Strategy to Create Glycan Analogs with Altered Biological Activities
著者名:Takahiro Moriyama, Makoto Yoritate, Naoki Kato, Azusa Saika, Wakana Kusuhara, Shunsuke Ono, Takahiro Nagatake, Hiroyuki Koshino, Noriaki Kiya, Natsuho Moritsuka, Riko Tanabe, Yu Hidaka, Kazuteru Usui, Suzuka Chiba, Noyuri Kudo, Rintaro Nakahashi, Kazunobu Igawa, Hiroaki Matoba, Katsuhiko Tomooka, Eri Ishikawa, Shunji Takahashi, Jun Kunisawa, Sho Yamasaki, and Go Hirai
D O I:10.1021/jacs.3c12581

企業プレスリリース詳細へ
PR TIMESトップへ
(2024/01/12 16:00)
- データ提供
-

本コーナーの内容に関するお問い合わせ、または掲載についてのお問い合わせは株式会社 PR TIMES ( )までご連絡ください。製品、サービスなどに関するお問い合わせは、それぞれの発表企業・団体にご連絡ください。
)までご連絡ください。製品、サービスなどに関するお問い合わせは、それぞれの発表企業・団体にご連絡ください。
 )までご連絡ください。製品、サービスなどに関するお問い合わせは、それぞれの発表企業・団体にご連絡ください。
)までご連絡ください。製品、サービスなどに関するお問い合わせは、それぞれの発表企業・団体にご連絡ください。