置換基が密集したベンゾフランを簡便合成する手法を開発 ~ベンゼン環上の置換基が隣接炭素に移動するユニークな反応機構~
東京理科大学
【研究の要旨とポイント】
活性化剤存在下でオルト置換フェノールとアルキニルスルホキシドを反応させることにより、多置換ベンゾフランを簡便に合成できる手法を開発しました。
本研究で発見した、ベンゼン環上の置換基が隣接炭素に移動するユニークな転位反応を利用し、さまざまな機能を有する多置換ベンゾフランを高収率で得ることができます。
本研究をさらに発展させることにより、合成が困難であった複雑なヘテロ環化合物を容易に合成することができ、創薬科学、医薬品合成、農学分野などの発展につながることが期待されます。
【研究の概要】
東京理科大学 先進工学部生命システム工学科の吉田 優准教授、同大学大学院 特別研究生の小林 瑛宏博士(2021年度~2023年度、2023年度 東京医科歯科大学大学院 博士課程修了)、同大学大学院 先進工学研究科生命システム工学専攻の田端 慎也氏(2023年度 修士課程修了)の研究グループは、トリフルオロ酢酸無水物(TFAA)存在下で、オルト位に置換基を持つフェノール類とアルキニルスルホキシドを反応させると、ベンゼン環上の置換基が隣接炭素に移動する特異的な反応が進行することを明らかにしました。また、この反応を利用することで、従来法では困難であった置換基が密集した多置換ベンゾフランを合成することに成功しました。
ベンゾフランをはじめとしたヘテロ環化合物には、生物活性など重要な性質を示すものがあり、有機化学や医薬品など、幅広い分野での利用が期待されています。しかしながら、これらの化合物の合成は難しく、従来法では高機能なヘテロ環化合物を得にくいという課題がありました。そこで本研究グループは、特異的な反応が期待できるカチオン性中間体を利用した反応設計を行い、多置換ベンゾフランの合成を達成すべく、研究を進めてきました。
本研究では、TFAA存在下でオルト置換フェノールとアルキニルスルホキシドを反応させることにより、ベンゼン環上の置換基の転位反応が進行し、簡便にベンゾフランの合成ができることを明らかにしました。また、原料のオルト置換フェノールとアルキニルスルホキシドを種々変更することにより、さまざまな置換基を有する多置換ベンゾフランを高い収率で得ることにも成功しています。
今回の特異的な反応機構を利用した手法により、従来法では合成困難であった置換基が密集したヘテロ環化合物を簡便に合成することができます。本研究成果をさらに発展させることにより、多様な機能を有する多置換ヘテロ環化合物を容易に得られるようになり、有機化学、医薬品、農薬などの広範な分野での研究の進展が期待されます。
本研究成果は、2024年3月28日に国際学術誌「Chemical Communications」にオンライン掲載されました。また、本論文は2024年に掲載されたものの中から、ホットな論文を集めたChemical Communications HOT Articles 2024にも選出され、世界から注目を集めています。
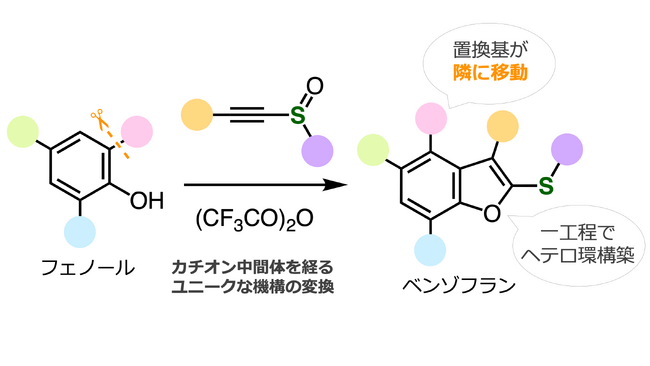
図 本研究の主要な反応
【研究の背景】
多置換ベンゼン上の置換基の移動反応は、置換基が密集した高機能なヘテロ環化合物を合成することができるため、注目を集めてきました。この置換基の移動反応では、反応途中で生成するカチオン中間体の転位反応が深く関わっていることが知られており、この機構を応用するための研究が広く行われてきました。しかしながら、この機構を組み込んだ化合物合成は依然として困難で、高機能なヘテロ環化合物合成を達成することができていませんでした。
これに対して本研究グループは、カチオン中間体の転位反応とそれに続く置換基の移動反応を利用した反応設計を行い、多置換ベンゾフランを合成する手法の開発を行いました。
【研究結果の詳細】
1. オルト置換フェノールとアルキニルスルホキシドによるベンゾフランの合成
はじめに、トリフルオロ酢酸無水物(TFAA)の存在下で、2-トリフルオロメチルフェノールとアルキニルスルホキシドを反応させると、立体障害の少ない部位でのC-C形成によって反応がスムーズに進行し、7-トリフルオロメチルベンゾフランを合成できることを明らかにしました。その一方で、原料として2-メチルフェノール(o-クレゾール)を用いると7-メチルベンゾフランと4-メチルベンゾフラン、2,5-ジメチルフェノールを用いると4,6-ジメチルベンゾフランと4,7-ジメチルベンゾフランが生成することがわかりました。これらの結果から、オルト位の置換基の立体障害を避けて、7-メチルベンゾフラン、4,7-ジメチルベンゾフランが生成すること、カチオン中間体の特異的な置換基移動の影響により、立体的に不利な4-メチルベンゾフランや4,6-ジメチルベンゾフランも生成することが示唆されました。
さらに本研究では、2,6-ジ置換フェノールやアルキニルスルホキシドを種々変更した検討も行っており、多様な置換基を有する多置換ベンゾフランの合成にも成功しています。一例として、2,3,5,6-テトラメチルフェノールをアルキニルスルホキシドと反応させると、すべての炭素原子が置換基を有する6置換ベンゾフランが生成することを明らかにしています。
2. 反応機構の詳細解明
反応機構の詳細を明らかにするため、TFAAの存在下で2,6-ジメチルフェノールと2,6-ジフェニルフェノールの等モル混合物をアルキニルスルホキシドで反応させたときの生成物に関する検討を行いました。その結果、主生成物として4,7-ジメチルベンゾフラン、副生成物として4,7-ジフェニルベンゾフランが得られることがわかりました。この結果から、電子供与性のメチル基を有する2,6-ジメチルフェノールが、電子求引性のフェニル基を有する2,6-ジフェニルフェノールよりも高い反応性を示すことが示唆されました。さらに、メチル基とフェニル基の両方を有するベンゾフランは検出されなかったため、分子内での置換基移動が重要であることが判明しました。
2,6-ジメチルフェノールを原料としたときの中間体を介した反応機構は以下の通りです。
(1): TFAAによるアルキニルスルホキシドの電子求核活性化により、スルホニウム中間体(中間体A)が生成
(2): 中間体Aと2,6-ジメチルフェノールの置換反応により、アルキニルスルホニウム中間体(中間体B)が生成
(3): 中間体Bの転位反応([3,3]-シグマトロピー転位)により、非芳香族化した中間体(中間体C)が生成
(4): 中間体CでのC-O形成(環閉鎖)、その後メチル基の移動と脱プロトン化によって、4,7-ジメチル置換ベンゾフランが生成
本研究を主導した吉田准教授は「カチオン性の中間体を経る反応系をデザインすることにより、通常は起こりえないような独特な反応が進行するようになると考え、本研究に取り組んできました。今回合成したベンゾフラン類は生物活性化合物の開発において重要です。本手法を応用することで、これまで合成が難しく生物活性等が知られていないベンゾフラン類を幅広く合成することができます。そのため、新しい構造の医農薬品の発見や開発の促進につながることが期待されます」と、研究成果についてコメントしています。
※本研究は、日本学術振興会(JSPS)の科研費(JP22H02086)、科学技術振興機構(JST)の次世代研究者挑戦的プログラム(SPRING, JPMJSP2120)、上原記念生命科学財団、徳山科学技術振興財団、UBE学術振興財団、稲盛財団の助成を受けて実施したものです。また、研究に使用したTf2Oはセントラル硝子株式会社から提供されました。
【論文情報】
雑誌名:Chemical Communications
論文タイトル:Highly substituted benzo[b]furan synthesis through substituent migration
著者:Akihiro Kobayashi, Shinya Tabata and Suguru Yoshida
DOI:10.1039/D4CC01192A
URL:https://doi.org/10.1039/D4CC01192A
企業プレスリリース詳細へ
PR TIMESトップへ
【研究の要旨とポイント】
活性化剤存在下でオルト置換フェノールとアルキニルスルホキシドを反応させることにより、多置換ベンゾフランを簡便に合成できる手法を開発しました。
本研究で発見した、ベンゼン環上の置換基が隣接炭素に移動するユニークな転位反応を利用し、さまざまな機能を有する多置換ベンゾフランを高収率で得ることができます。
本研究をさらに発展させることにより、合成が困難であった複雑なヘテロ環化合物を容易に合成することができ、創薬科学、医薬品合成、農学分野などの発展につながることが期待されます。
【研究の概要】
東京理科大学 先進工学部生命システム工学科の吉田 優准教授、同大学大学院 特別研究生の小林 瑛宏博士(2021年度~2023年度、2023年度 東京医科歯科大学大学院 博士課程修了)、同大学大学院 先進工学研究科生命システム工学専攻の田端 慎也氏(2023年度 修士課程修了)の研究グループは、トリフルオロ酢酸無水物(TFAA)存在下で、オルト位に置換基を持つフェノール類とアルキニルスルホキシドを反応させると、ベンゼン環上の置換基が隣接炭素に移動する特異的な反応が進行することを明らかにしました。また、この反応を利用することで、従来法では困難であった置換基が密集した多置換ベンゾフランを合成することに成功しました。
ベンゾフランをはじめとしたヘテロ環化合物には、生物活性など重要な性質を示すものがあり、有機化学や医薬品など、幅広い分野での利用が期待されています。しかしながら、これらの化合物の合成は難しく、従来法では高機能なヘテロ環化合物を得にくいという課題がありました。そこで本研究グループは、特異的な反応が期待できるカチオン性中間体を利用した反応設計を行い、多置換ベンゾフランの合成を達成すべく、研究を進めてきました。
本研究では、TFAA存在下でオルト置換フェノールとアルキニルスルホキシドを反応させることにより、ベンゼン環上の置換基の転位反応が進行し、簡便にベンゾフランの合成ができることを明らかにしました。また、原料のオルト置換フェノールとアルキニルスルホキシドを種々変更することにより、さまざまな置換基を有する多置換ベンゾフランを高い収率で得ることにも成功しています。
今回の特異的な反応機構を利用した手法により、従来法では合成困難であった置換基が密集したヘテロ環化合物を簡便に合成することができます。本研究成果をさらに発展させることにより、多様な機能を有する多置換ヘテロ環化合物を容易に得られるようになり、有機化学、医薬品、農薬などの広範な分野での研究の進展が期待されます。
本研究成果は、2024年3月28日に国際学術誌「Chemical Communications」にオンライン掲載されました。また、本論文は2024年に掲載されたものの中から、ホットな論文を集めたChemical Communications HOT Articles 2024にも選出され、世界から注目を集めています。

図 本研究の主要な反応
【研究の背景】
多置換ベンゼン上の置換基の移動反応は、置換基が密集した高機能なヘテロ環化合物を合成することができるため、注目を集めてきました。この置換基の移動反応では、反応途中で生成するカチオン中間体の転位反応が深く関わっていることが知られており、この機構を応用するための研究が広く行われてきました。しかしながら、この機構を組み込んだ化合物合成は依然として困難で、高機能なヘテロ環化合物合成を達成することができていませんでした。
これに対して本研究グループは、カチオン中間体の転位反応とそれに続く置換基の移動反応を利用した反応設計を行い、多置換ベンゾフランを合成する手法の開発を行いました。
【研究結果の詳細】
1. オルト置換フェノールとアルキニルスルホキシドによるベンゾフランの合成
はじめに、トリフルオロ酢酸無水物(TFAA)の存在下で、2-トリフルオロメチルフェノールとアルキニルスルホキシドを反応させると、立体障害の少ない部位でのC-C形成によって反応がスムーズに進行し、7-トリフルオロメチルベンゾフランを合成できることを明らかにしました。その一方で、原料として2-メチルフェノール(o-クレゾール)を用いると7-メチルベンゾフランと4-メチルベンゾフラン、2,5-ジメチルフェノールを用いると4,6-ジメチルベンゾフランと4,7-ジメチルベンゾフランが生成することがわかりました。これらの結果から、オルト位の置換基の立体障害を避けて、7-メチルベンゾフラン、4,7-ジメチルベンゾフランが生成すること、カチオン中間体の特異的な置換基移動の影響により、立体的に不利な4-メチルベンゾフランや4,6-ジメチルベンゾフランも生成することが示唆されました。
さらに本研究では、2,6-ジ置換フェノールやアルキニルスルホキシドを種々変更した検討も行っており、多様な置換基を有する多置換ベンゾフランの合成にも成功しています。一例として、2,3,5,6-テトラメチルフェノールをアルキニルスルホキシドと反応させると、すべての炭素原子が置換基を有する6置換ベンゾフランが生成することを明らかにしています。
2. 反応機構の詳細解明
反応機構の詳細を明らかにするため、TFAAの存在下で2,6-ジメチルフェノールと2,6-ジフェニルフェノールの等モル混合物をアルキニルスルホキシドで反応させたときの生成物に関する検討を行いました。その結果、主生成物として4,7-ジメチルベンゾフラン、副生成物として4,7-ジフェニルベンゾフランが得られることがわかりました。この結果から、電子供与性のメチル基を有する2,6-ジメチルフェノールが、電子求引性のフェニル基を有する2,6-ジフェニルフェノールよりも高い反応性を示すことが示唆されました。さらに、メチル基とフェニル基の両方を有するベンゾフランは検出されなかったため、分子内での置換基移動が重要であることが判明しました。
2,6-ジメチルフェノールを原料としたときの中間体を介した反応機構は以下の通りです。
(1): TFAAによるアルキニルスルホキシドの電子求核活性化により、スルホニウム中間体(中間体A)が生成
(2): 中間体Aと2,6-ジメチルフェノールの置換反応により、アルキニルスルホニウム中間体(中間体B)が生成
(3): 中間体Bの転位反応([3,3]-シグマトロピー転位)により、非芳香族化した中間体(中間体C)が生成
(4): 中間体CでのC-O形成(環閉鎖)、その後メチル基の移動と脱プロトン化によって、4,7-ジメチル置換ベンゾフランが生成
本研究を主導した吉田准教授は「カチオン性の中間体を経る反応系をデザインすることにより、通常は起こりえないような独特な反応が進行するようになると考え、本研究に取り組んできました。今回合成したベンゾフラン類は生物活性化合物の開発において重要です。本手法を応用することで、これまで合成が難しく生物活性等が知られていないベンゾフラン類を幅広く合成することができます。そのため、新しい構造の医農薬品の発見や開発の促進につながることが期待されます」と、研究成果についてコメントしています。
※本研究は、日本学術振興会(JSPS)の科研費(JP22H02086)、科学技術振興機構(JST)の次世代研究者挑戦的プログラム(SPRING, JPMJSP2120)、上原記念生命科学財団、徳山科学技術振興財団、UBE学術振興財団、稲盛財団の助成を受けて実施したものです。また、研究に使用したTf2Oはセントラル硝子株式会社から提供されました。
【論文情報】
雑誌名:Chemical Communications
論文タイトル:Highly substituted benzo[b]furan synthesis through substituent migration
著者:Akihiro Kobayashi, Shinya Tabata and Suguru Yoshida
DOI:10.1039/D4CC01192A
URL:https://doi.org/10.1039/D4CC01192A
企業プレスリリース詳細へ
PR TIMESトップへ
(2024/04/16 10:00)
- データ提供
-

本コーナーの内容に関するお問い合わせ、または掲載についてのお問い合わせは株式会社 PR TIMES ( )までご連絡ください。製品、サービスなどに関するお問い合わせは、それぞれの発表企業・団体にご連絡ください。
)までご連絡ください。製品、サービスなどに関するお問い合わせは、それぞれの発表企業・団体にご連絡ください。
 )までご連絡ください。製品、サービスなどに関するお問い合わせは、それぞれの発表企業・団体にご連絡ください。
)までご連絡ください。製品、サービスなどに関するお問い合わせは、それぞれの発表企業・団体にご連絡ください。