2025/06/03 11:41
口腔がんの診断数、著名人のがん公表後に約1.5倍に
[概要]
新型コロナ後遺症でみられる脳内炎症や倦怠感などの脳神経症状の発症メカニズムは不明でしたが、東京慈恵会医科大学・ウイルス学講座(講座担当教授:近藤一博)は、新型コロナウイルスのスパイクタンパク質の一部であるS1タンパク質が鼻腔内で発現するだけで、これらの脳神経症状が生じることを発見しました。
また、S1タンパク質を発現させた新型コロナ後遺症モデルマウスは脳内のアセチルコリンの産生が低下しており、認知症の治療薬であるドネペジル(商品名:アリセプト)を投与して脳内のアセチルコリン不足を補うことで、脳内炎症や倦怠感が改善されることを見出しました。
本研究の成果は、新型コロナ後遺症の脳内炎症や倦怠感の原因がスパイクタンパク質の一部であるS1タンパク質の鼻腔内発現であることを示し、ドネペジルによる治療の可能性を示唆します。
また、このようなスパイクタンパク質の鼻腔内発現による病原性とその発症機構を明らかにしたことで、現在、世界中で計画されている、鼻腔投与を中心とした次世代新型コロナワクチンの安全性を向上させる方法の開発にも貢献できるものと考えています。
本研究は、日本医療研究開発機構(AMED) 新興・再興感染症に対する革新的医薬品等開発推進研究事業の支援(研究開発課題名:新型コロナウイルス感染症(COVID-19)の後遺症として生じるうつ症状と疲労の予防および治療を目指した発生機構解明)によって行われ、2023年5月24日付で米国科学誌iScience(Cell press)に掲載されました。
[研究背景]
COVID-19の重症化や死亡者は減少していますが、これに代わって新型コロナ後遺症の増加が問題となっています。特に問題となっているのは、勤労の妨げや生活の質の低下に直結する脳内炎症や倦怠感などの脳神経関連の症状です。通常のウイルスではこのような症状は、ウイルスが脳で増殖することにより生じます。しかし、新型コロナウイルスは脳で増殖するという明確な証拠がないために、脳内炎症や倦怠感が生じる原因が不明で、治療法も判りませんでした。本研究は、このような問題に解答を与えるものです。
新型コロナウイルスの感染防止のためには、感染予防効果が高く、接種の際の痛みなどの副反応の少ない次世代新型コロナワクチンの開発が進められています。その有力候補として期待されているのが、鼻からワクチンを投与する経鼻ワクチンです。しかし、現行のワクチン抗原であるスパイクタンパク質を利用した経鼻ワクチンは倦怠感などの副反応が意外に強く、開発は期待どおりには進んでいません。本研究は、このような問題の原因究明となり、解決策を与えるものでもあります。
[今後の展開]
ドネペジルの臨床治験は、本研究の成果をもとに、現在、AMED新興・再興感染症に対する革新的医薬品等開発推進研究事業の支援の基、横浜市立大学、聖マリアンナ医科大学、慈恵医大などの共同研究で実施中です。
また、本研究により、鼻腔内でスパイクタンパク質(S1タンパク質)が発現すると脳内炎症や新型コロナ後遺症の原因となり得ることが判りました。スパイクタンパク質を利用する経鼻ワクチンは、これと同様の危険性を含んでいると考えられます。今回の我々の研究では、スパイクタンパク質がどのようなメカニズムで脳内炎症や新型コロナ後遺症を引き起こすことも明らかにしているため、この成果を利用して、スパイクタンパク質の病原性を取り除くことにより、安全性の高い経鼻ワクチンの開発が可能になると考えられます。
[研究成果の詳細]
1. 新型コロナ後遺症モデルマウスの作製
従来のSARS-CoV-2を感染させた動物モデルでは感染動物が短期間で死亡してしまうので、新型コロナ後遺症の症状を呈するモデル動物を作製することはできませんでした。そこで我々は、SARS-CoV-2のタンパク質を発現するアデノウイルスベクターを鼻腔内に投与することで、新型コロナ後遺症の症状を現すモデルマウスを作製することを試みました。その結果、SARS-CoV-2スパイクタンパク質のS1領域のタンパク質を導入したマウス(S1マウス)が、倦怠感の指標である重り付き強制水泳時間の短縮と、うつ症状の指標である尾懸垂試験における無動時間の延長を呈したため(図1)、S1マウスが新型コロナ後遺症の倦怠感とうつ症状のモデルマウスとなると考えられました。
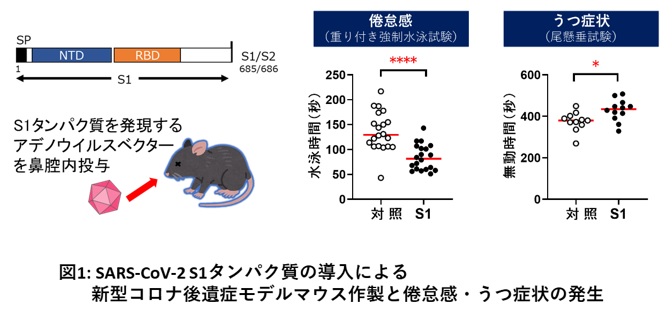
図1
2. 新型コロナ後遺症モデルマウスの脳機能解析
新型コロナ後遺症の発症機構を解明するために、新型コロナ後遺症のモデルマウスであるS1マウスの脳機能異常について調べました。その結果、嗅覚障害の原因となり得る嗅球細胞のアポトーシス増加や、倦怠感・うつ症状の原因となる脳の炎症(炎症性サイトカインIL-6の産生亢進)が見られることが判りました(図2上段)。
これらの機能障害が生じる原因を明らかにするために脳の神経伝達物質を検討したところ、内側中隔野や対角帯と呼ばれる、本来アセチルコリン産生が活発な部位でアセチルコリン産生細胞が減少していることが判りました(図2下段)。
アセチルコリンは、コリン作動性抗炎症反応と呼ばれる作用を通じて、脳や末梢臓器の炎症を抑制することが知られています。このことから、我々は新型コロナ後遺症で見られる倦怠感やうつ症状は、脳内のアセチルコリンが不足することで脳内炎症が抑えられないために生じるのではないかと考えました。
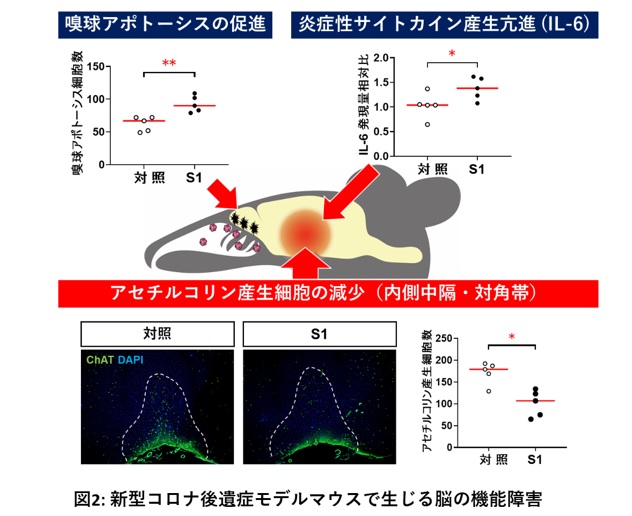
図2
3. ドネペジルによる治療
新型コロナ後遺症の倦怠感やうつ症状が脳内のアセチルコリン不足による脳内炎症によるという仮説を証明し、この仮説に基づく治療法を開発するために、我々は、アセチルコリンの分解を阻害して、脳内のアセチルコリン濃度を上昇させる働きを持つドネペジルを、S1マウスに投与しました。ドネペジルの投与量は動物実験での標準的な量である体重1Kgあたり4mgを1週間、飲水に混ぜて与えました。
この結果、脳内炎症(炎症性サイトカインIL-6の産生亢進)はドネペジル投与によって解消し図3左)、また倦怠感の指標である水泳時間の短縮や、うつ症状の指標である無動時間の延長も認められなくなりました(図3中、右)。
これらの結果は、新型コロナ後遺症の原因が脳内のアセチルコリン不足による脳内炎症であることを示すとともに、この現象がドネペジルの投与によって治療可能であることを示すものと考えられました。
図3
[論文]
SARS-CoV-2 S1 protein causes brain inflammation by reducing intracerebral acetylcholine production
Naomi Oka, Kazuya Shimada, Azusa Ishii, Nobuyuki Kobayashi, Kazuhiro Kondo*
Department of Virology, The Jikei University School of Medicine, 3-25-8 Nishi-Shimbashi, Minato-ku, Tokyo 105-8461, Japan. * Correspondence: kkondo@jikei.ac.jp
iScience (Cell press) 電子版 5月24日掲載
(2023/05/29 15:52)
2025/06/03 11:41
口腔がんの診断数、著名人のがん公表後に約1.5倍に
2025/06/02 10:57
治療タンパク質を脳へ輸送する新たな遺伝子治療法を開発
2025/05/26 12:34
H1抗ヒスタミン薬の注意すべき副作用と発症時期を特定
~日本人リアルワールドデータを用いて調査~