東京理科大学大学院理学研究科化学専攻の手島涼太氏らは、海岸に漂着した海藻から抽出したアルギン酸塩と炭酸カルシウム(CaCO3)の混合水溶液に炭酸水を加える簡便な方法で、従来の創傷治療用ゲルと真逆の性質である「低接着性・低膨潤性」を有する創傷治療用ゲルを開発したとInt J Biol Macromol(2023; 254: 127928)に報告した。高い創傷治療効果を有し、従来の創傷治療用ゲルで生じる創傷部の一時的な拡張を防げることから、環境にも配慮した新たなゲルとしての実用化が期待される。
CaCO3濃度の異なる3種のゲルを合成
ハイドロゲルは皮膚組織からの滲出液を吸収する性質に加え、湿潤環境を維持して創傷治癒を促進する性質を持つことから、近年多くの創傷治療用ゲルに使用されている。創傷治療用ゲルの設計には、①皮膚の動きに追従するための接着性、②滲出液を吸液するための膨潤性-が必要と考えられてきたが、ハイドロゲルが皮膚に接着した状態で滲出液を吸収し膨張すると、創傷部も一緒に引っ張られて拡張を引き起こす危険性がある。しかし、このような創傷部拡張への対策は十分に講じられておらず、ハイドロゲルの接着性・膨潤性と創傷部の拡張についての関連を明らかにし、より高い機能を有する創傷治療用ゲルの開発が求められていた。
手島氏らはこれまでに、アルギン酸を原料としたハイドロゲルが創傷治療に応用可能な材料であることを報告している(Polym Adv Technol 2020; 31: 3032-3038)。今回、創傷治療用ゲルとしての実用化を目指して研究を進めた。
まず同氏らは、アルギン酸カリウムと濃度が異なるCaCO3(0.15 w/v%、0.20 w/v%、0.30w/v%)の混合溶液を作製し炭酸水を加えることで、3種のアルギン酸ゲル(Alg-Ca0.15、Alg-Ca0.20、Alg-Ca0.30)を調製した。走査型電子顕微鏡による観察やゲル強度を測定した結果、全てのアルギン酸ゲルが三次元の網目構造を形成しており、変形に強いことが分かった。また、CaCO3濃度の上昇はゲルの透明性や架橋度の低下と関連していた。
続いて、ヒト皮膚線維芽細胞(NHDF)を用いて、アルギン酸ゲルの生体適合性と細胞接着性を評価したところ、全てのアルギン酸ゲルでNHDF生存率がほぼ100%だった。さらに、組織培養ポリスチレンプレート上で培養したNHDFは細長く伸びて接着していたのに対し、アルギン酸ゲル上で培養したNHDFは細胞が凝集して三次元構造となるスフェロイドを形成しており、アルギン酸ゲルの表面では細胞接着性が低かった。これらの結果から、アルギン酸ゲルが創傷被覆材として十分に高い生体適合性と低細胞接着性を有していることが示された。
SDGsに配慮した次世代医療用素材のベンチマークに
そこで、Alg-Ca0.20と臨床使用されているハイドロゲル創傷治療材ビューゲルのマウス皮膚組織に対する接着性および膨潤性を比較したところ、Alg-Ca0.20に比べビューゲルは11.9~16.5倍の皮膚接着率を有し、生理食塩水の吸収に伴う重量変化率はAlg-Ca0.20の1.9倍と高く、Alg-Ca0.20の低接着性・低膨潤性が実証された。
最後に、アルギン酸ゲルの低皮膚接着性・低膨潤性創傷治療材としての有効性を確認するため、Alg-Ca0.20とビューゲルを創傷モデルマウスに貼付し、創傷治癒効果を評価した。ハイドロゲルをマウスの創傷部位に固定し、創傷面積の変化を経時的に測定したところ、両者の創傷治癒効果に有意差はなく、Alg-Ca0.20はビューゲルと同等の治療効果を有することが示唆された。また、ビューゲルした創傷部の面積は、高い接着性と膨潤性による一時的な拡大が観察された。これは、治癒の初期段階に多量の滲出液が産生されてゲルが大きく膨潤したことが原因と考えられるが、Alg-Ca0.20で被覆した創傷部では拡張が抑制された。これまでの創傷治療用ゲルと真逆の特性である低接着性・低膨潤性により、ゲルの膨潤が引き起こす創傷部の拡張を抑制することが示唆された(図)。
図.アルギン酸ゲルの特徴
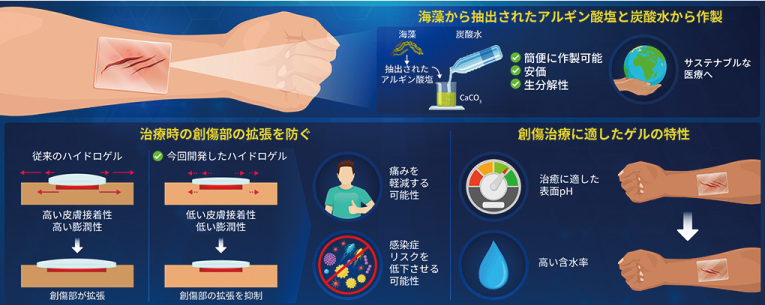
(東京理科大学プレスリリースより)
手島氏は「実臨床における創傷被覆材の課題に着目し、海藻という廃棄されていた原料を活用することで高機能な創傷治療用ゲルを開発できた。医療用素材にはまだまだ持続可能な開発目標(SDGs)の視点が不足している。本研究が次世代の医療用素材の設計におけるベンチマークの1つになると期待したい」と展望している。
(編集部)






















