2025/06/23 17:55
ISHA 2025へようこそ!
ISHA – 国際股関節保存学会は、2025年10月2日から4日まで、日本の…
東京慈恵会医科大学 薬理学講座 西條琢真博士研究員(現:愛知県医療療育総合センター 発達障害研究所 分子病態研究部門)、鈴木江津子講師、籾山俊彦教授らのグループは、二種類のセロトニン受容体がそれぞれ異なった様式でアルツハイマー型認知症と密接に関係する前脳基底核(注1)内の興奮性シナプス伝達を調節していることを明らかにしました。
今回の研究によりアルツハイマー型認知症など認知・記憶機能におけるセロトニン受容体の役割やアルツハイマー型認知症とうつ病が併発する仕組みについて理解が進み、新たな治療法の開発につながることが期待されます。
本研究成果は「Journal of Physiology」に掲載されました(2022年7月1日, volume600, issue 13)。
~ 研究成果のポイント ~
Ø 今回の研究では、二種類のセロトニン受容体が、それぞれ異なるメカニズムにより前脳基底核コリン作動性ニューロンへの興奮性シナプス伝達を調節していることが明らかになりました。
Ø 今回の研究によりアルツハイマー型認知症など認知・記憶機能におけるセロトニン受容体の役割やアルツハイマー型認知症とうつ病が併発する仕込みの理解が進み、新たな治療法の開発が期待されます。
研究背景
アルツハイマー型認知症は日本国内における認知症患者の67.6%を占め、将来的にはさらに増加することが予想されています(注2)。アセチルコリンという物質は認知機能、記憶や睡眠サイクルなどに関連する重要な神経伝達物質です。アルツハイマー型認知症では脳内のアセチルコリンが減少することが知られており、認知症の進行を遅らせる治療薬は、脳内のアセチルコリン濃度を上昇させるものが主流となっています(注3)。
前脳基底核という脳の領域には、脳内に広くアセチルコリンを放出するコリン作動性ニューロンという神経細胞が多く存在しています。コリン作動性ニューロンはアルツハイマー型認知症患者では減少していることが知られており、またこの前脳基底核という脳領域を損傷した方では健忘という記憶障害が生じます。
前脳基底核内には背側縫線核という脳領域から、セロトニンという、うつ病や不安障害といった精神疾患と関連する物質が放出されています。アルツハイマー型認知症とうつ病は併発することもあり、セロトニンがどのように前脳基底核コリン作動性ニューロンの活動に影響するのかを明らかにすることは二つの疾患のクロスポイントを知る上で重要です。これまでに研究グループでは、数種類あるセロトニン受容体(サブタイプ)のうち、セロトニン5-HT1B受容体の作用により前脳基底核コリン作動性ニューロンへの抑制性神経伝達が抑制されることを明らかにしました(注4)。このセロトニン5-HT1B受容体による抑制性神経伝達の抑制は、シナプス前部からの神経伝達物質放出が抑制されるためでした。一方で興奮性シナプス伝達に対するセロトニンの調節作用は明らかとなっていませんでした。
研究内容
研究グループは、げっ歯類の脳から前脳基底核を含むスライス標本を作製し、コリン作動性ニューロンから電気生理学的手法を用いて記録される興奮性シナプス電流に対するセロトニンの作用を検討しました。前脳基底核コリン作動性ニューロンから興奮性シナプス電流を記録する際に細胞外にセロトニンを与えると、興奮性シナプス電流が抑制されることがわかりました(図1)。
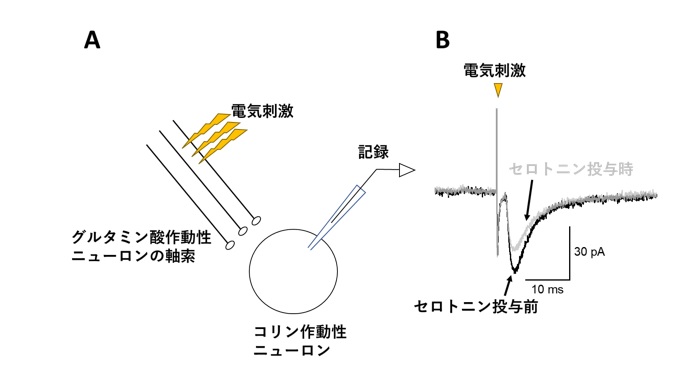
図1.セロトニンは興奮性シナプス電流を抑制する
A.電気生理学的手法の模式図。前脳基底核のコリン作動性ニューロン周辺に刺激電極を配置し、人工的にグルタミン酸作動性ニューロンの軸索を活性化させることで軸索終末部からの神経伝達物質(ここではグルタミン酸)の放出を促す。放出されたグルタミン酸は、前脳基底核コリン作動性ニューロンの細胞膜上に発現するグルタミン酸受容体に結合する。コリン作動性ニューロンから細胞内に流入するイオンにより生じる電流を測定する。
B. コリン作動性ニューロンから記録された電流例を示す。黒色線はセロトニンを細胞外に投与する前の電流応答を、灰色線はセロトニン投与後の電流応答である。セロトニン投与により電流の振幅が小さくなっている。L字型のスケールは、細胞応答の大きさを示す縦軸の電流変化(pA;ピコアンペア)と時間の幅(ms;ミリ秒)を示す。
セロトニンがどのようなメカニズムにより、興奮性シナプス伝達を調節するのか、セロトニン受容体の各サブタイプ特異的な阻害薬を用いて検討しました。その結果、セロトニン5-HT1B受容体はシナプス前細胞からの神経伝達物質(グルタミン酸)の放出を抑制し、5-HT1A受容体はシナプス後細胞に発現するグルタミン酸受容体(AMPA受容体とNMDA受容体)に作用することが判明しました。一種類の神経伝達物質による調節作用が、二つの異なる受容体を介し、またそれぞれ異なるメカニズムにより生じることが明らかとなりました(図2)。
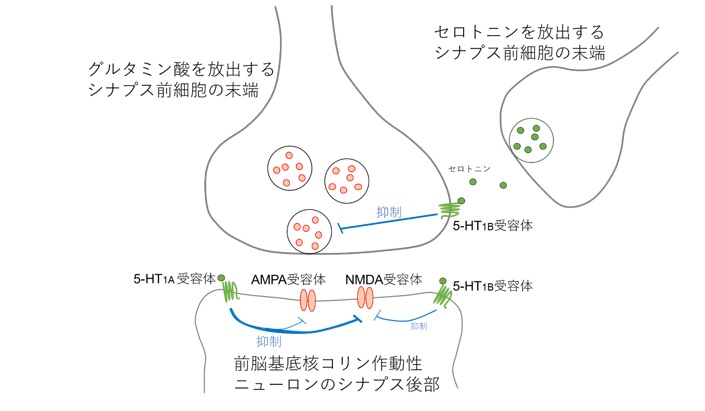
図2.前脳基底核コリン作動性ニューロンへの興奮性シナプス伝達が
セロトニンにより抑制されるメカニズム
解説:前脳基底核コリン作動性ニューロンへの興奮性シナプス伝達では、シナプス前部の細胞からグルタミン酸が放出される。放出されたグルタミン酸は、シナプス後部であるコリン作動性ニューロンの細胞膜上にあるグルタミン酸受容体(AMPA受容体およびNMDA受容体)に結合し、コリン作動性ニューロンを興奮させる。背側縫線核の神経細胞から放出されたセロトニンは、シナプス前部の5-HT1B受容体に結合してグルタミン酸の放出を抑制し、シナプス後部の5-HT1A受容体に結合して主にNMDA受容体のグルタミン酸への感受性に作用する。
本研究の社会的意義
前脳基底核コリン作動性ニューロンは脳全体にアセチルコリンを広く放出する重要な神経細胞であり、アルツハイマー型認知症との関連が指摘されています。アルツハイマー型認知症患者では、うつ病の併発も知られており、アルツハイマー型認知症とうつ病との関連性を明らかにすることは、アルツハイマー型認知症患者の生活の質(QOL)を支えるうえで重要です。研究グループのこれまでの研究と本研究により、うつ病との関連が指摘される神経伝達物質であるセロトニンが、前脳基底核コリン作動性ニューロンの興奮・抑制のバランスを制御していることが明らかとなりました。このようなアセチルコリンとセロトニンの関係性がわかることで、今後アルツハイマー型認知症患者におけるうつ病併発のメカニズム、さらには新たな治療法開発に関する研究が進むことが期待されます。
研究費
本研究は、科研費(17K07063, 19K23370)および上原記念生命科学財団の支援を受けて実施されました。
論文情報
Nishijo T*, Suzuki E* & Momiyama T, 2022, Serotonin 5-HT1A and 5-HT1B receptor-mediated inhibition of glutamatergic transmission onto rat basal forebrain cholinergic neurons, Journal of Physiology, 6, 3149-3167.
DOI: https://doi.org/10.1113/JP282509
*These authors contributed equally to the study.
注釈と用語解説
(注1)
前脳基底核は前頭葉の底部の後方に位置する神経細胞の集まり(核)です。特にコリン作動性ニューロンの起始核として、脳内に広くアセチルコリンを放出しています。
(注2)
厚生労働省老健局発表資料(令和元年6月20日)
https://www.mhlw.go.jp/content/12300000/000519620.pdf
(注3)
認知症疾患診療ガイドライン2017(一般社団法人 日本神経学会)
(注4)
Nishijo T & Momiyama T, 2016, Serotonin 5-HT1B receptor-mediated calcium influx-independent presynaptic inhibition of GABA release onto rat basal forebrain cholinergic neurons. European journal of Neuroscience, 44, p1747-1760.
(2022/07/11 13:51)
2025/06/23 17:55
ISHA 2025へようこそ!
ISHA – 国際股関節保存学会は、2025年10月2日から4日まで、日本の…
2025/06/06 12:24
第14回日本認知症予防学会学術集会
この度、第14回日本認知症予防学会学術集会の大会長を拝命いたしま…