2025/06/23 17:55
ISHA 2025へようこそ!
ISHA – 国際股関節保存学会は、2025年10月2日から4日まで、日本の…
研究成果の概要
本研究では、特発性肺線維症の患者が、SARS-CoV-2感染により高感受性である事を示した。一方急性肺炎時、肺腔内におけるウイルス感染可能な領域は、むしろ狭まる傾向にあり、感染に対し抵抗性を獲得するという結論を示した。
今回のデータが、「SARS-CoV-2感染に対し、特発性肺線維症患者の重症化リスクは高い」という結論に直接結びつくものではないが、肺腔内におけるSARS-CoV-2感染可能領域がより広がっていることから、警戒すべき疾患であると考える必要がある。
【背景】
特発性肺線維症の患者は、SARS-CoV-2感染に対し、より高い感受性を有するのではないかと危惧されていた。またSARS-CoV-2感染により引き起こされる急性肺炎によるサイトカインストームが、肺腔内で発現しているACE2(SARS-CoV-2感染の細胞内への入り口となるアンジオテンシン変換酵素2)の発現量を上昇させ、感染領域を広げる可能性が示唆されていた。
そこで我々が独自に開発した特発性肺線維症マウスモデル(iUIPモデル)および患者サンプルを用い肺腔内におけるACE2発現に関する研究を進めた。また感染により引き起こされる病態生理学的状態を、PCLS(肺臓の薄切組織)を用いたex vivo培養システムの中で再現し、肺におけるACE2発現の変化を検証した。
【研究の成果】
本研究により慢性的な肺線維症状態にある特発性肺線維症では、ACE2の発現量が非病態時より多いことからSARS-CoV-2感染のリスクが高いことが分かった。一方急性炎症化期、ACE2の発現量はむしろ減少することが分かった。このことから急性炎症期、肺腔内における感染領域はむしろ減少している事が示唆された(図1参照)。
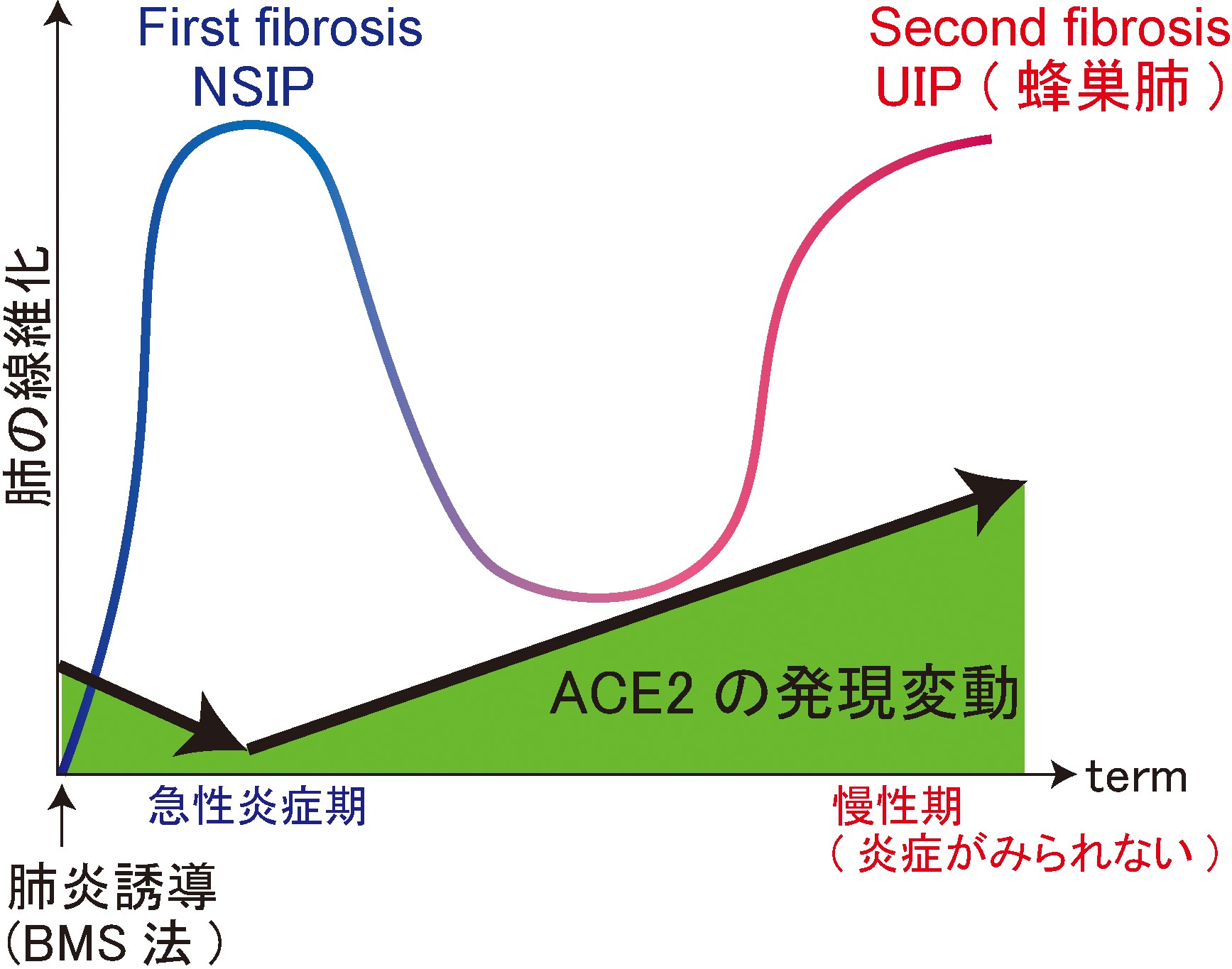
図1
図1 iUIP(誘導性特発性肺線維症)マウスモデルにおける線維化とACE2発現量の変化 ヒト患者検体においてもマウスモデル同様のACE2発現の上昇が観察された。
iUIPマウスモデルにおいて肺炎慢性期、浸潤性を獲得した異常な上皮細胞が観察される(Miura et al. LSA. 2022, 2022名古屋市立大学プレスリリース参照)事が分かった。この異常上皮細部の約20%でACE2発現が観察された。これらの上皮細胞では、上皮細胞自身の極性が消失している可能性が示唆された(細気管支領域ではACE2発現は気道面に発現している、一方浸潤性を獲得した異常上皮細胞では、ACE2発現に一定の方向性が見られない)。特発性肺線維症の患者肺においても肥厚した上皮細胞に加え、浸潤性の上皮細胞も確認される。これらの上皮細胞でもマウスモデル同様、異所性のACE2発現が観察された(図2参照)。
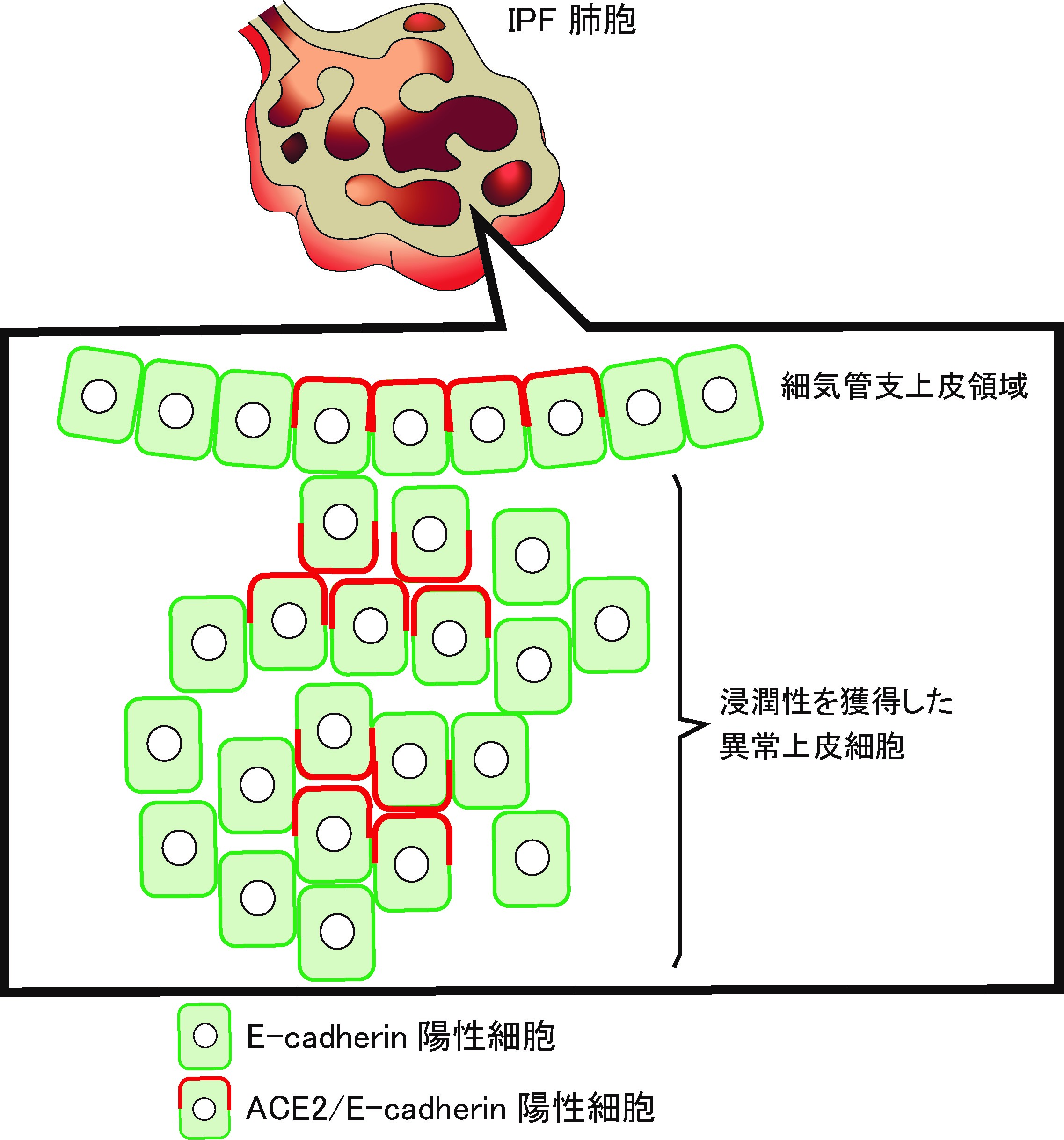
図2
図2 特発性肺線維症において浸潤性を獲得した異常上皮細胞が観察され、これらの細胞の一部においてACE2の発現が見られる。
急性炎症時、肺におけるACE2発現量が下がる理由を探るため、SARS-CoV-2感染時の病態生理学的状態(各種サイトカイン、低酸素状態)が肺に及ぼす影響をPCLS, ex vivo培養システムを用い検討した。
COVID19治療に関するニュース(関節リウマチ治療薬を転用できるかもしれないとの観測)などで話題になったインターロイキン6、ウイルス感染により誘導産生されるインターフェロン、ウイルス感染そのもの(実験ではウイルス感染状態を疑似的に再現している)によってACE2の発現量はむしろ減少することが明らかになった。また間質性肺炎下で肺は低酸素状態になると考えられているが、このような低酸素環境もACE2発現量を減少させることが分かった。また間質性肺炎治療に用いられる代表的な治療薬、ピルフェニドン、ニンテダニブが、ACE2発現に影響を及ぼすのか否かについても検討した。ピルフェニドン投与による影響は見られなかった一方、ニンテダニブ投与によりACE2発現量が減少することが分かった。
Precision-cut lung slices (PCLS)を用いたex vivo培養の樹立
今回の研究では、特発性肺線維症マウスモデル (induced-usual interstitial pneumonia, iUIP, 特発性間質性肺炎)由来のPCLSを用い研究を進めた。PCLSは、肺組織そのものを薄切したもので、PCLSに関する一連の研究はモナーシュ大学(メルボルン、オーストラリア)との共同研究で進めている。
今後この技術を応用し、肺に対する毒性試験、抗がん剤による線維化の評価、肺線維症に対する治療薬開発など多岐に渡る応用研究を進めていく予定である(図3参照)。
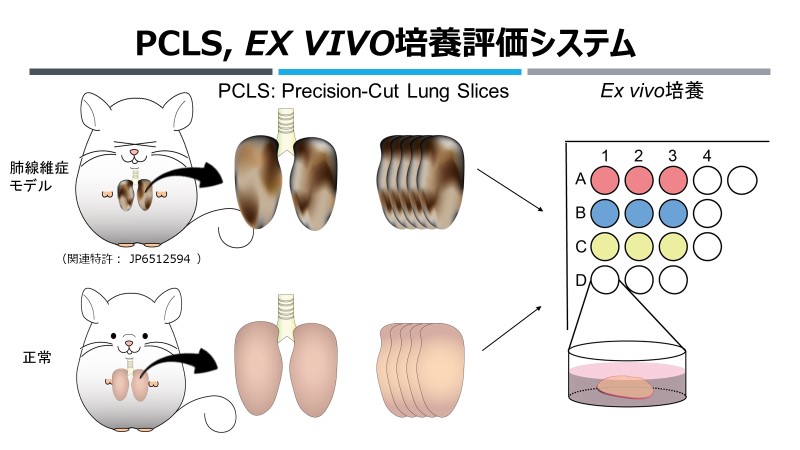
図3
図3 PCLS, ex vivo培養評価システム
【研究のポイント】
・特発性肺線維症の患者では、SARS-CoV-2レセプター、ACE2の発現量が健常人に比べ高いことから、SARS-CoV-2感染をより受けやすい可能性があることを示した。
・一方急性炎症を伴う肺炎では、ACE2の発現量はむしろ減少するが明らかになった。
・ACE2は、異常性を獲得した上皮細胞において発現していることを見いだした。
・特発性肺線維症モデルマウス由来のPCLSを用いたex vivo培養システムを樹立した。このシステムを利用することで、使用する動物の数を減らし、より効率的に作用物による肺への影響を評価することができることを示した。
【研究の意義と今後の展開や社会的意義など】
我々が開発したiUIPマウスモデルは、肺に強い炎症を引き起こした後にIPF様の症状を呈する。このマウスモデルと患者検体を用い、特発性肺線維症ではSARS-CoV-2感染リスクが高い可能性を示した。
SARS-CoV-2感染治療薬の開発は、ワクチン開発に対し、大きく立ち遅れている。今回の研究成果には、新たな治療薬開発のヒントとなるデータが多く含まれている。特に、PCLS、ex vivo培養システムは、感染症の治療薬開発だけでなく、間質性肺炎治療薬開発、肺に対する毒性試験など重要な検討項目を評価するための、強力なツールになる可能性がある。
【用語解説】
SARS-CoV-2 新型コロナ感染症(COVID19)の原因ウイルスで、日本では「新型コロナウイルス」と呼ばれる。
Pathophysiological conditions “病態生理学的状態“を意味する。論文では疑似的なSARS-CoV-2感染状態、感染後のインターフェロン、サイトカイン、線維化に関わる因子、低酸素状態などさまざまなウイルス感染状態を総称する意味で使用している。
ex vivo培養 ex vivoは生体外を意味する。論文では肺由来のPCLSを培養することを意味する。
ACE2 (Angiotensin Converting Enzyme 2、アンジオテンシン変換酵素2) SARS-CoV-2によるヒトへの感染は、ACE2を介し行われる。このため、ACE2はウイルスが細胞の中へ入り込む際の最初の入り口(レセプター)として機能する。本来の機能は、ACEとともに血管の拡張、弛緩(しかん)を制御する機能を持つ。
注)本リリースでは、全てACE2と表記している。このためACE2(ヒト)、Ace2(マウス)等の区別をしていません。
特発性肺線維症 特発性肺線維症は、国の指定難病とされていて「特発性間質性肺炎」の1種に分類されている。英語ではIdiopathic Pulmonary Fibrosis(IPF)と表記され、肺胞に“傷”ができ、その修復のためにコラーゲン産生等が増加し、その結果肺の間質部が厚くなる病気と考えられている。「特発性」とは、発症原因が不明であることを意味するが、疫学解析から喫煙との関連性が高く、高齢の男性で多く発症する等のリスク要因は確定されている。
PCLS(Precision-Cut Lung Slices)薄切した肺臓で、この薄切片を用いさまざまな検討を行うことができる。ex vivo培養を行うことで、一度に多くの情報を得ることが可能となる。
【研究助成】
・文部科学省・日本学術振興会科学研究費補助金(JP17K16055)
・GSKジャパン研究助成2018
・日東学術振興財団2020
・個人寄付 古屋 徹氏
・オーストラリア国立保健医療研究評議会(APP1165690, APP1187755)
・JST START 大学・エコシステム推進型 スタートアップ・エコシステム形成支援、JPMJST 2183
【論文タイトル】
Pathophysiological conditions induced by SARS-CoV-2 infection reduce ACE2 expression in the lung.
(日本語タイトル) SARS-CoV-2感染により引き起こされる病態生理学的状態はACE2(SARS-CoV-2レセプター)の発現を減少させる
【著者】
Yoko Miura1, Hirotsugu Ohkubo2, Akiko Nakano2, Jane E. Bourke3, and Satoshi Kanazawa1
三浦陽子1、大久保仁嗣2、中野暁子2, ジェーン・バーク3、金澤智1
【所属】
1 Department of Neurodevelopmental Disorder Genetics, Nagoya City University
Graduate School of Medical Sciences, Nagoya, Aichi, Japan
名古屋市立大学 大学院医学研究科 神経発達症遺伝学
2 Department of Respiratory Medicine, Allergy and Clinical Immunology, Nagoya City University Graduate School of Medical Sciences, Nagoya, Aichi, Japan
名古屋市立大学 大学院医学研究科 呼吸器・免疫アレルギー内科学
3 Department of Pharmacology, Biomedicine Discovery Institute, Monash University, Clayton, Australia
【掲載学術誌】
学術誌名:Frontiers in Immunology
DOI番号:10.3389/fimmu.2022.1028613
【研究に関する問い合わせ】
名古屋市立大学 大学院医学研究科
脳神経科学研究所 神経発達症遺伝学分野 助教 金澤 智
住所:名古屋市瑞穂区瑞穂町字川澄1
TEL:052-853-8205
E-mail:kanas@med.nagoya-cu.ac.jp
【報道に関する問い合わせ】
名古屋市立大学 病院管理部経営課経営係
名古屋市瑞穂区瑞穂町字川澄1
TEL:052-858-7113 FAX:052-858-7537
E-mail:hpkouhou@sec.nagoya-cu.ac.jp
(2022/11/11 14:25)
2025/06/23 17:55
ISHA 2025へようこそ!
ISHA – 国際股関節保存学会は、2025年10月2日から4日まで、日本の…
2025/06/06 12:24
第14回日本認知症予防学会学術集会
この度、第14回日本認知症予防学会学術集会の大会長を拝命いたしま…