2025/06/23 17:55
ISHA 2025へようこそ!
ISHA – 国際股関節保存学会は、2025年10月2日から4日まで、日本の…


医師や病気・症状、ニュースなどが検索できます
東京慈恵会医科大学細菌学講座の杉本真也准教授と金城雄樹教授は、難治性感染症の発症や水浄化システムの機能低下などの原因となる微生物の集合体であるバイオフィルム(注1)を、内部の微生物が生きたままの状態で瞬時に透明にして顕微鏡で観察する世界初の新技術iCBiofilm(アイ・シー・バイオフィルム)法(注2)を開発しました。
従来の光学顕微鏡法では、光の散乱や屈折によりバイオフィルムの表面から20マイクロメートル程度の深さまでしか観察できず、その全体像や内部の微細な構造を観察することは極めて困難でした(文献1、2)。iCBiofilm法は、500マイクロメートルを超えるような分厚いバイオフィルムでも観察することが可能であり、世界最高性能の深部イメージングを実現しました。また、iCBiofilm法を応用することで、微生物が生きたままの状態で透明にすることが可能になり、その形成過程や抗菌物質の殺菌作用を詳しく解析できるようになりました。それらにより構造や機能に対する理解が飛躍的に高まり、これまで困難とされてきた難治性バイオフィルム感染症治療法の開発や水浄化システムの高効率化など、さまざまな分野での社会実装につながると期待されます。
研究成果の概要
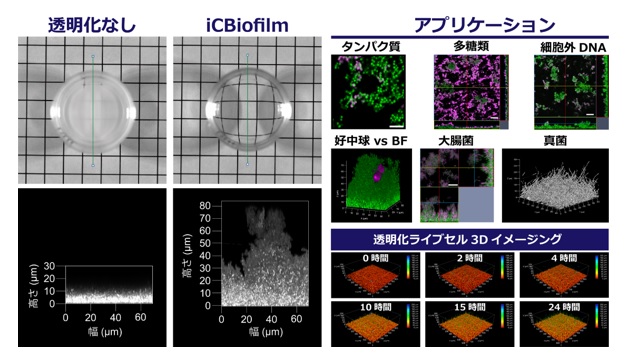
①バイオフィルムを生きたままの状態で瞬時(数秒以内)に透明にできるiCBiofilm法を開発し、製品化しました。
②iCBiofilm法はさまざまな微生物(細菌および真菌)のバイオフィルムに使用でき、その構成成分(微生物細胞、タンパク質、多糖類、DNAなど)の分布を、空間配置を壊さず可視化できます。
③iCBiofilm法は、従来の組織透明化法では不可能であった透明化3Dライブセルイメージングを実施することも可能であり、バイオフィルムの形成過程や抗菌物質の作用を解析できます。
今後の取り組み
今回の研究成果を医学の分野で活用し、ヒトの組織表面や体内に埋め込まれた医療デバイスに形成されたバイオフィルムの観察を現在進めています。また、本研究成果は水浄化システムのろ過膜の表面、住環境(バスタブや台所)、および発酵食品の製造過程などで形成されたバイオフィルムの観察にも応用できると考えています。さらに、今回の研究成果をもとに、スフェロイドやオルガノイドなどの動植物細胞の集塊のようなバイオフィルム以外の生体試料も透明化できる「3Dライブセルイメージング法」の開発を目指した新たなプロジェクトを立ち上げる予定です。なお、本研究成果をもとにしたバイオフィルム透明化試薬「iCBiofilm―H1」および「iCBiofilm―H2」は、東京化成工業株式会社より製品化されています。
本研究の成果は2023年1月23日19時(日本時間)、Communications Biology誌に掲載されます。
論文情報
タイトル:Instantaneous Clearing of Biofilm (iCBiofilm): an optical approach to revisit bacterial and fungal biofilm imaging
著者 :Shinya Sugimoto and Yuki Kinjo
掲載誌 :Communications Biology(2023年1月23日にオンライン掲載)
Doi :10.1038/s42003-022-04396-4
本研究は、戦略的創造研究推進事業(ERATO)「野村集団微生物制御プロジェクト」(JPMJER1502)、文部科学省科学研究費補助金 基盤研究(B)(20H02904)、同 新学術領域研究「超地球生命体を解き明かすポストコッホ機能生態学」(22H04889)、東京慈恵会医科大学 戦略的重点配分研究費、および住友科学財団研究助成金などの助成を受けて行われました。
研究メンバー:
・東京慈恵会医科大学 細菌学講座 准教授 杉本 真也
細菌学講座 教授 金城 雄樹
研究の詳細
1.背景
微生物の集合体であるバイオフィルムは水の浄化や発酵食品の製造など、人類の生活を支える重要な機能を持っています。その一方で、バイオフィルムを形成した病原菌が感染症やう蝕(虫歯)を引き起こすように、人類にとって負の側面も持っています。特に、中心静脈カテーテルや人工関節などの血管留置型医療デバイスに形成されると、バイオフィルムの内部の病原菌が抗菌薬やヒトの免疫による排除機能に抵抗性を示すようになるため、感染症は治療が難しくなってしまいます。その場合、医療デバイスを取り除く必要があり、患者への負担と医療費が大きくなるという問題があります。そのような事態を回避するためには、バイオフィルムのことを深く理解し、バイオフィルムを作らせないようにしたり、出来上がったバイオフィルムを取り除いたり、部分的にバイオフィルムを壊して抗菌薬が働きやすくするなど、バイオフィルムを制御する方法を開発する必要があります。
生命現象を理解する上で、顕微鏡を使って対象とする生物を観察することは最も基本的かつ重要なアプローチの一つです。特に、バイオフィルムが作られるメカニズムや抗菌物質、免疫に対する抵抗性などを理解するためには、その構造や内部における微生物の生理状態、遺伝子発現、代謝物の変動、構成成分などを顕微鏡で詳しく観察することが不可欠です。これまで、50マイクロメートルを超えるような分厚いバイオフィルムには光が深部まで透過しにくいため、従来の光学顕微鏡法(共焦点レーザー顕微鏡(注3)、超解像顕微鏡(注4)、多光子顕微鏡(注5)など)では隅々まで観察することは困難でした。よって、形状は変化させずに鮮明に観察することができる革新的な顕微鏡観察技術の創出が求められていました。
2.研究手法と成果
これまでに動物の組織や臓器を透明化して顕微鏡で観察する技術(組織透明化技術)が開発されていました。そこで本研究グループは、既存の組織透明化技術(CUBIC(注6)、ScaleS(注7)、SeeDB2(注8))を用いてメチシリン耐性黄色ブドウ球菌(MRSA)(注9)のバイオフィルムの透明化を試みました。しかし、従来の組織透明化法は①透明度が不十分である、②透明化処理の過程で界面活性剤などの脂質除去作用などによりバイオフィルムの構造が部分的に壊されてしまう、③透明化処理に数日から数週間の時間を要する、という問題に直面しました。その一方で、SeeDB2に含まれる「イオヘキソール」という化合物のみを含む水溶液にMRSAのバイオフィルムを浸漬させると、バイオフィルムが瞬時に透明になることを発見しました。イオヘキソールは水によく溶け、屈折率が極めて高いという特徴を持ちますが、水溶液中の濃度を変えることで屈折率を自在に調整することが可能です。そこで本研究グループは、イオヘキソールを基に、透明度が高く、バイオフィルムの構造安定性に優れた条件を決め、500マイクロメートルを超えるような分厚いバイオフィルムでも瞬時(数秒以内)に透明にするiCBiofilm(アイ・シー・バイオフィルム)法を開発しました。
従来の組織透明化法の場合、組織や臓器に含まれる光の散乱や吸収の原因となる物質(繊維状タンパク質、脂質、および色素など)を取り除き、周囲の溶媒の屈折率を観察対象の屈折率に近づける工程で長い処理時間を要します。一方、iCBiofilm法はバイオフィルムを構成する微生物細胞の屈折率(1.38~1.42程度)に近い溶媒(イオヘキソール溶液など)に浸漬するだけで数秒以内に透明化を達成できる圧倒的に処理時間の短い方法です(透明化試薬を添加した直後にバイオフィルムが透明になっていく様子はオンライン論文上のムービーで閲覧できます)。従来の組織透明化法(CUBIC、ScaleS、SeeDB2など)に比べて透明度が高く、より深部まで鮮明に観察できるようになりました(図1)。また、蛍光標識抗体や蛍光色素で染色したMRSAのバイオフィルムをiCBiofilm法で透明にすることで、バイオフィルム内部の微生物細胞やマトリクスの構成成分(タンパク質、細胞外多糖、細胞外DNA)(文献3)の微細な構造や局在を、共焦点レーザー顕微鏡などを用いて深部まで詳しく観察することが可能になりました(図2)。iCBiofilm法は、MRSAのバイオフィルムだけでなくさまざまな細菌(注10)や真菌(注11)の透明化にも応用することが可能でした。これにより、従来は底面に酵母型の丸い細胞が層をなし、その上部に菌糸型の線維状の細胞が存在すると考えられてきた真菌の一種であるCandida albicansのバイオフィルムが、実は底面にも菌糸型の細胞が多数存在し、酵母型の細胞はわずかであることもわかりました(図3)。また、MRSAの成熟したバイオフィルムに好中球(注12)を一定時間作用させ、透明化処理なしで観察すると、好中球がバイオフィルムの上部に浮遊しているように観察されていましたが、iCBiofilm法を用いることで好中球がバイオフィルムの内部まで侵入し、黄色ブドウ球菌を貪食していることが明らかになりました(図4)。
従来の組織透明化法は試料を固定した後、透明化するのに数日から数週間の時間を要するため、生物を生きたままの状態で透明にして観察することは不可能でしたが、iCBiofilm法に使用する試薬の種類と濃度を最適化することで、バイオフィルム内部の微生物を生きたままで透明にしながら3次元で観察すること(透明化3Dライブセルイメージング)が可能になりました。iCBiofilm法に使用していたイオヘキソールは未固定のMRSAのバイオフィルム構造にダメージを与えるため、透明化ライブセルイメージングには適しませんでしたが、新たに高い透明化能と低い侵襲性を併せ持つ化合物として、イオジキサノールを見いだしました。イオジキサノールは微生物の細胞分裂や形態に影響しないことから、細胞毒性は極めて低い化合物です。バイオフィルムを形成させるために使用する培地の中に適切な濃度のイオジキサノールと細胞に対する毒性が低い蛍光プローブ(注13)を添加することで、形成過程の透明化3Dライブセルイメージングが可能になりました(図5:論文にはムービーも掲載)。これにより、MRSAのバイオフィルムが抗菌物質(乳酸菌が産生するナイシンAという抗菌ペプチド)によって殺菌されていく様子も観察できるようになりました(図6:論文にはムービーも掲載)。
3.今後の展開
本研究で開発したiCBiofilm法をさまざまな光学顕微鏡(ラマンスペクトル顕微鏡、自家蛍光顕微鏡、超解像顕微鏡、ライトシート顕微鏡、多光子顕微鏡)と組み合わせることで、バイオフィルムの詳細な構造に加え、微生物細胞の生理状態、代謝物の分布など機能面の情報が高い空間分解能で得られると考えられます。これにより構造や機能をより深く理解できるようになり、バイオフィルムが原因となる難治性細菌感染症の予防法や治療法の開発にもつながる可能性があります。また、バイオフィルムは水処理や発酵食品の製造など人類に恩恵をもたらすことも多く、良い面と悪い面を含めた新たな制御技術の開発は社会的・経済的にもインパクトが大きいため、本技術の波及効果は極めて大きいと考えられます。
4.参考図
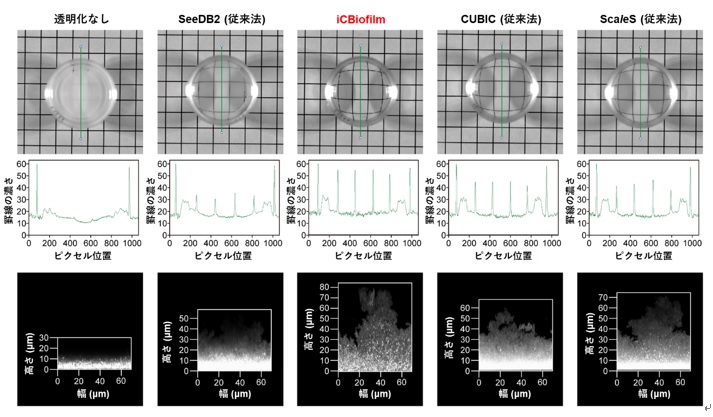
図1
図1.iCBiofilm法と従来の組織透明化法の比較
上段:ガラス底培養皿の中でMRSA臨床分離株のバイオフィルムを形成後、上記の透明化法で処理し、培養皿をけい線の掛かれた白紙の上に載せて写真を撮影した。中段:上段の写真のうち、培養皿の後ろ側の黒いけい線の濃さを緑の線上で計測し、グラフ化した。下段:MRSAのバイオフィルムを、RNAを染色するチオフラビンT(文献4)で染め、倒立型共焦点レーザー顕微鏡を用いて観察した。透明化処理なしの場合は、下部から照射したレーザー光が表面近くまでしか届かないため、ガラス表面近くの細胞しか観察できていない。従来の組織透明化法でも改善がみられるが、iCBiofilm法が最も透明度が高く、バイオフィルムの底部から上部までくまなく観察できている。従来法は、底面付近は鮮明に観察できているが、上部に行くに従って光の散乱が起き、蛍光の明るさが低下していく。
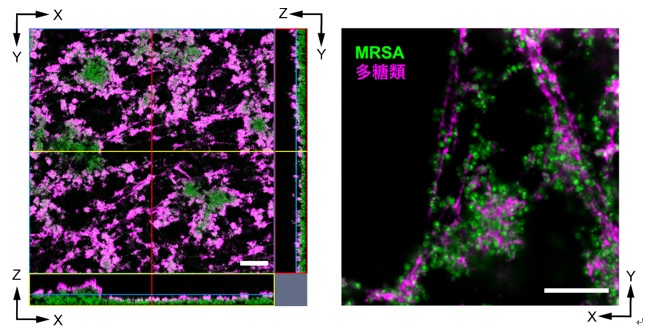
図2
図2.MRSAのバイオフィルムを構成する細胞外多糖類の観察
MRSAを細胞膜親和性のFM1-43(緑)で、細胞外多糖類をAlexa Fluor 647で標識したWheat germ agglutinin(マゼンタ)で染色し、iCBiofilm法で透明化した後に共焦点レーザー顕微鏡を用いて観察した。左図:バイオフィルムのXY、XZ、YZ断面像。バイオフィルムの上部を多糖類が覆っている。スケールバーは50マイクロメートル。右図:細胞外多糖類が線維状のネットワーク構造を形成している。スケールバーは10マイクロメートル。
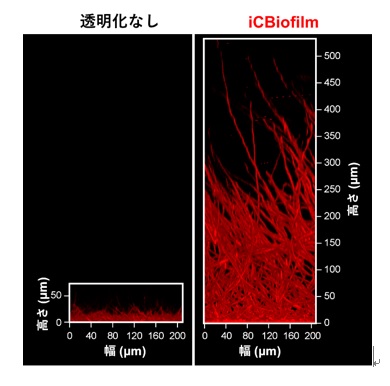
図3
図3.病原性真菌Candida albicansのバイオフィルムの観察
細胞壁を染色するAlexaFluor 594で標識したConcanavalin Aで染色後、透明化なし、もしくはiCBiofilm法で透明化し、共焦点レーザー顕微鏡を用いて観察した。
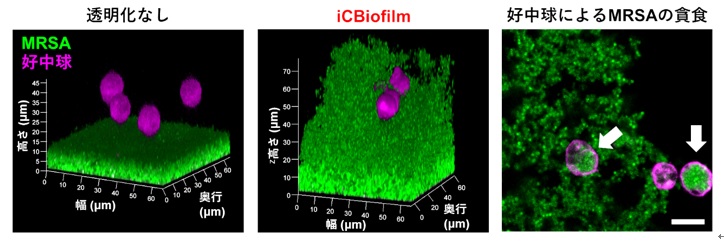
図4
図4.MRSAバイオフィルムと好中球の相互作用の観察
左図:透明化なしで観察するとMRSAのバイオフィルム(緑)の上部に好中球(マゼンタ)が浮遊しているように見える。中央図:iCBiofilm法を用いて透明化した後に観察すると上部まで鮮明に観察でき、好中球が内部まで侵入している様子がわかる。右図:XY断面図。好中球の一部がバイオフィルム内部のMRSAを貪食している(白矢印)。
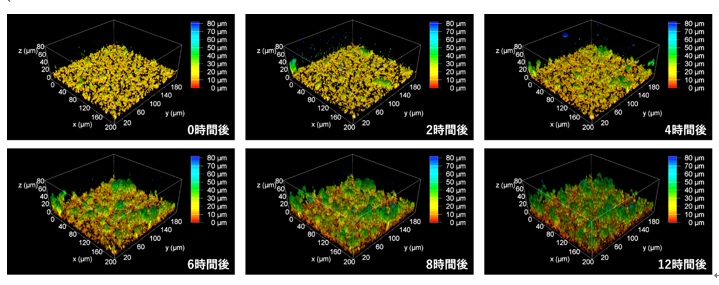
図5
図5.MRSAのバイオフィルム形成の透明化3Dライブセルイメージング
最適な濃度に調整したイオジキサノールと蛍光色素(MitoTracker DeepRed)を添加したバイオフィルム形成用の培地にMRSAを接種し、ガラス底培養皿の中で培養しながら10分おきに3次元の蛍光画像を取得した。色はバイオフィルムの高さを示している。オンラインでムービーを閲覧できる。
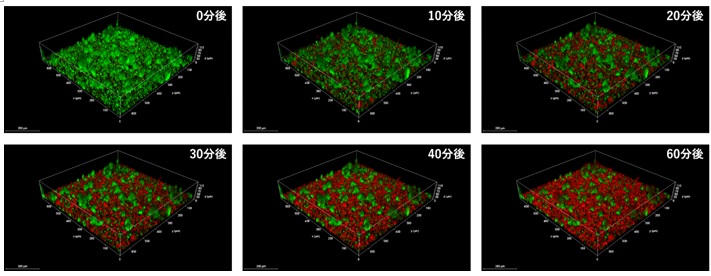
図6
図6.MRSAのバイオフィルムに対する抗菌ペプチドの殺菌作用の透明化3Dライブセルイメージング
MRSAのバイオフィルムをガラス底培養皿で形成させた。その後、培養液を取り除き、そこに生菌を染めるSyto9(緑)、死菌を染めるPropidium Iodide(赤)、および抗菌ペプチド(ナイシンA)(文献5)を添加したPBSを加え、1分おきに3次元画像を取得した(一部の画像のみを掲載)。オンラインでムービーを閲覧できる。
5.用語説明
(注1)バイオフィルム
微生物が固相表面に形成した集合体。花瓶の内壁や流しなど地球環境で水のあるところにみられる粘着物など、細菌が形成する生物膜のこと。
(注2)iCBiofilm(アイ・シー・バイオフィルム)法
instantaneous Clearing of Biofilm(瞬間的バイオフィルム透明化)の略称。「アイ・シー・バイオフィルム」という読み方は「I see biofilm(バイオフィルムを見る)」に由来する。
(注3)共焦点レーザー顕微鏡
小さく絞ったレーザー光を走査して画像を取得する走査型蛍光顕微鏡の一種。蛍光シグナルを検出する際、焦点位置以外の光は点光源(ピンホール)で除去されるため、深さ方向に分解能が生じ、光学的断層像を得ることができる。そのため、光を全面に照射する一般の顕微鏡と違って厚い試料でもピントを合わせた蛍光像を得ることが可能。
(注4)超解像顕微鏡
光学顕微鏡で観察できる空間分解能は、観察に用いる光の波長の半分程度(200ナノメートル程度)であることが理論的に示されている。近年、この限界を超えるイメージングの方法がいくつか考案されており、これらの技術をまとめて超解像顕微鏡法と呼ぶ。例えば、構造化照明顕微鏡法、誘導放出抑制顕微鏡法、光活性化局在性顕微鏡法などがある。超解像顕微鏡法では 100 ナノメートル以下、場合によっては数ナノメートルの分解能を達成できる。
(注5)多光子顕微鏡
蛍光顕微鏡の1種。特殊な赤外光パルスレーザーを用いることで、ピントの合った深度でだけ蛍光色素を光らせることができるため、鮮明な像を得ることができ、深さを少しずつ変えながら撮像していくことで3次元蛍光画像を得ることができる。共焦点顕微鏡と比べると、光散乱の影響を受けにくい長波長のレーザーを使うため、より深くまで可視化することが可能。
(注6)CUBIC
Clear,Unobstructed Brain Imaging Cocktails and Computational analysisの略。2014年4月に理化学研究所 生命システム研究センターの上田泰己博士らが発表した脳透明化と全脳イメージングのための透明化試薬(アミノアルコール、タンパク質変性作用のある尿素、界面活性剤であるTriton X―100の混合溶液)とコンピューター画像解析を合わせた方法。1細胞解像度の全脳蛍光イメージングと、情報科学的解析によるサンプル間のシグナル比較法を実現している。
(注7)ScaleS
2015年に理化学研究所 脳科学総合研究センターの宮脇敦史博士らによって開発された透明化法。糖アルコールの一種であるソルビトールと尿素、およびTriton X-100を主成分とする。蛍光タンパク質の退色が少ない、脳がほとんど膨張しない、細胞膜が保持される、抗原性が保持されるなどの特徴がある。
(注8)SeeDB2
2016年に理化学研究所(現九州大学医学研究院)の今井猛博士らが開発した組織透明化法。X線の造影剤の一種であるイオヘキソールと界面活性剤であるサポニンを主成分とし、簡便で組織形態にやさしいという特徴を持つ。イオヘキソールはCTスキャンで血管などの構造を可視化するために副作用の少ないX線造影剤として開発されたヨウ素を含む芳香族化合物である。ヨウ素がX線をよく吸収するため、X線造影剤として医療目的で用いられてきた。
(注9)黄色ブドウ球菌
基本的には、一部の健康な人にも存在する常在菌。しかし、バイオフィルムを形成しやすく、時に致死的な感染症を起こす病原細菌にもなる。特に、メチシリンという抗菌薬に耐性を有するメチシリン耐性黄色ブドウ球菌(MRSA:methicillin―resistant Staphylococcus aureus)がしばしば院内感染を引き起こし、問題となっている。最近では、侵襲性の高い市中感染型MRSAによる劇症型感染症も問題となっている。
(注10)細菌
目には見えない直径数マイクロメートル程度の微生物であり、核を持たない原核生物に分類される。黄色ブドウ球菌、大腸菌、腸球菌、枯草菌など、さまざまな細菌がバイオフィルムを形成する。ヒトの皮膚や腸管に常在する常在細菌や、さまざまな感染症を引き起こす病原細菌の存在が知られている。
(注11)真菌
動植物と同様に核を持つ真核生物に分類される微生物。カンジダ属やアスペルギルス属などの病原性真菌がバイオフィルムを形成し、難治性感染症の原因となる。
(注12)好中球
白血球のひとつであり、外部から侵入した細菌などの病原体を貪食する作用を持つ。これまではバイオフィルムの内部の細菌は好中球によって貪食されにくいと考えられていた。
(注13)蛍光プローブ
特定の分子と反応すると分子構造が変化し、強い蛍光を発したり、蛍光の色調が変化したりする機能性分子。
6.引用文献
1. Redundant and Distinct Roles of Secreted Protein Eap and Cell Wall-Anchored Protein SasG in Biofilm Formation and Pathogenicity of Staphylococcus aureus. Yonemoto K, Chiba A, Sugimoto S, Sato C, Saito M, Kinjo Y, Marumo K, Mizunoe Y. Infect Immun. 2019 Mar 25;87(4):e00894-18. doi: 10.1128/IAI.00894-18.
2. Staphylococcus aureus utilizes environmental RNA as a building material in specific polysaccharide-dependent biofilms. Chiba A, Seki M, Suzuki Y, Kinjo Y, Mizunoe Y, Sugimoto S. npj Biofilms Microbiomes. 2022 Apr 4;8(1):17. doi: 10.1038/s41522-022-00278-z.
3. Broad impact of extracellular DNA on biofilm formation by clinically isolated Methicillin-resistant and -sensitive strains of Staphylococcus aureus. Sugimoto S, Sato F, Miyakawa R, Chiba A, Onodera S, Hori S, Mizunoe Y. Sci Rep. 2018 Feb 2;8(1):2254. doi: 10.1038/s41598-018-20485-z.
4. Thioflavin T as a fluorescence probe for monitoring RNA metabolism at molecular and cellular levels. Sugimoto S, Arita-Morioka K, Mizunoe Y, Yamanaka K, Ogura T. Nucleic Acids Res. 2015 Aug 18;43(14):e92. doi: 10.1093/nar/gkv338.
5. Effects of bacteriocins on methicillin-resistant Staphylococcus aureus biofilm. Okuda K, Zendo T, Sugimoto S, Iwase T, Tajima A, Yamada S, Sonomoto K, Mizunoe Y. Antimicrob Agents Chemother. 2013 Nov;57(11):5572-9. doi: 10.1128/AAC.00888-13.
以上
(2023/01/24 10:52)
2025/06/23 17:55
ISHA 2025へようこそ!
ISHA – 国際股関節保存学会は、2025年10月2日から4日まで、日本の…
2025/06/06 12:24
第14回日本認知症予防学会学術集会
この度、第14回日本認知症予防学会学術集会の大会長を拝命いたしま…