2025/06/23 17:55
ISHA 2025へようこそ!
ISHA – 国際股関節保存学会は、2025年10月2日から4日まで、日本の…
東京慈恵会医科大学 腎臓・高血圧内科 松井賢治助教、横尾隆教授、山中修一郎助教(兼任:プロジェクト研究部腎臓応用再生医学研究室 室長)らの研究グループは、人工的アポトーシス誘導技術を動物モデルに応用し、世界で初めて、臓器形成初期の前駆細胞を選択的に除去することで、慢性腎臓病(CKD)の病態を再現することに成功しました。
この技術により、高効率・迅速・安全な手法による腎不全モデルマウス(動物モデル)の開発が可能になりました。
本研究で用いた人工的アポトーシス誘導技術は、従来の細胞除去の手法と比較して除去速度が極めて速く、除去率も94%という高い効率を実現しました。さらに、誘導剤の安全性が高いため、母体や胎仔への有害事象のリスクを大幅に低減できました。
本研究は、これまで困難であった胎仔期における病態制御を、高効率・迅速・安全に実現し、再現性の高い腎不全モデルを確立しました。作製されたモデル動物はCKDの進行に重要な糸球体過剰濾過の病態を忠実に再現しており、CKDのメカニズム解明や新規治療法開発に大きく貢献することが期待されます。
さらに、本技術はキメラ腎臓研究への応用も見据え、異種移植・再生医療分野への貢献も期待されます。異種動物由来の部分を除去してヒト臓器へ置換することで、拒絶反応のリスクを低減した再生腎臓の作製に応用できる可能性があり、腎不全の新たな治療戦略となることが期待されます。また、生まれながらに重症度の高い腎不全モデルをレシピエントモデルとして用いることでポッター症候群などの治療開発にも応用可能と考えます。
本研究成果は、国際科学雑誌 『Nature Communications』 オンライン版(3月15日付)に掲載されました。
【研究の背景】
慢性腎臓病(CKD)は、日本国内に約1,330万人の患者がいるとされる国民病であり(注1)、進行すると透析や腎移植が必要となる深刻な疾患です。効果的な治療法開発のためには、CKDの発症メカニズムや病態進行の過程を詳しく解明することが不可欠です。
動物モデルは、疾患研究において非常に重要なツールですが、従来のモデルには限界がありました。特に、胎仔期から発症する腎不全のモデルを作製することは技術的に困難であり、研究の大きな障壁となっていました。
また、近年注目されている異種移植・再生医療領域においても、拒絶反応の問題を克服し、機能的な臓器を効率的に作製する技術が求められています。
【研究の成果】
本研究グループは、これまでの課題を克服するため、細胞死を人工的に誘導するシステムである「誘導性Caspase9 (iCaspase9)」に着目しました。そして、iCaspase9を動物に組み込んだモデルとして、通称「ATTAC9[アタックナイン]:Apoptosis Through Targeted Activation of Caspase9」を作製し提案しています。
この技術は、プログラムされた細胞死の一種であるアポトーシスにおいて、内因性アポトーシス経路の主要な実行因子であるCaspase9に着目し、人工的に作製された誘導剤と結合するiCaspase9を細胞に組み込むことで、誘導剤の投与に応じてアポトーシス経路を活性化し、標的細胞を迅速かつ効率的に除去することを可能にします。
今回、研究グループはiCaspase9をマウスに応用したSix2-ATTAC9マウスを開発しました。腎臓の元となるSix2陽性ネフロン前駆細胞を選択的にアポトーシス誘導することに成功し、ATTAC9システムが胎仔臓器への細胞除去性能に優れていることを明らかにしました。その結果、以下の画期的な成果が得られました(図1)。
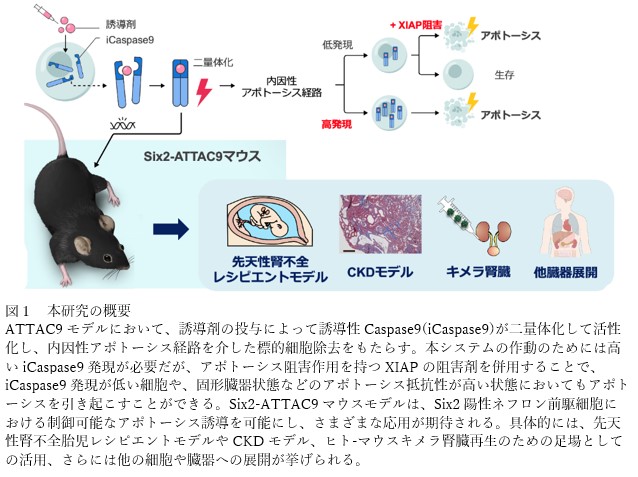
1.人工的アポトーシス誘導による腎不全モデルの作製
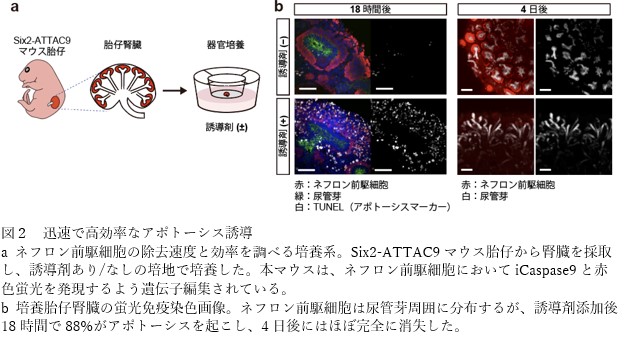
ATTAC9モデルは従来の細胞除去手法と比較して、細胞除去速度、除去効率、安全性において優位性を示し(図2)、胎仔および母体への負担を大幅に軽減しました。
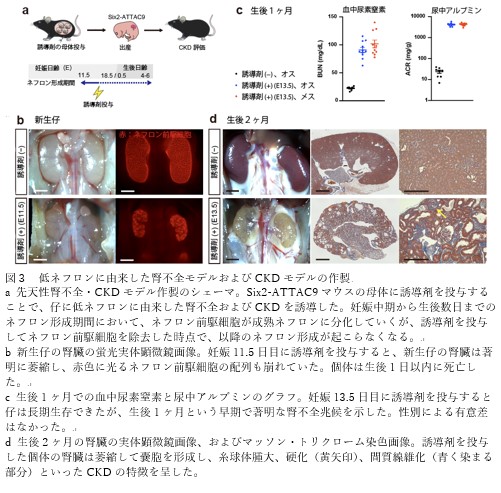
妊娠中の母体に誘導剤を投与することで、胎仔のネフロン前駆細胞を迅速かつ高効率に減少させ、腎不全を発症させることに世界で初めて成功しました(図3)。本研究グループは、近年進展する異種移植研究において、世界に先駆けて先天性腎不全の胎児を対象とした異種胎仔腎移植による治療法を提唱しています(注2)。本モデルはその研究のためのレシピエントモデルとしての活用可能性も秘めています。
2.糸球体過剰濾過モデルの確立とCKD病態の再現
妊娠時期が進むにつれて臓器発生が進み、ネフロン前駆細胞は成熟腎細胞に分化していくため、誘導剤の投与時期を遅らせることで腎不全は軽度となります。本システムの効率性・迅速性という利点を活かし、投与時期の調整のみによって再現性高く腎不全の重症度を調整することが可能となりました。特に妊娠13.5日目に投与した胎仔は出生後も生存可能であり、慢性的な腎機能障害を詳細に観察することができました。このマウスはヒトのCKD患者と同様に、糸球体の腫大や硬化、間質の線維化、炎症細胞の浸潤といった特徴を示しました(図3)。これは、残された腎機能で老廃物を濾過しようとする糸球体過剰濾過という病態を再現していることを示唆しており、CKDの進行メカニズム解明に非常に有用なモデルとなることが期待されます。
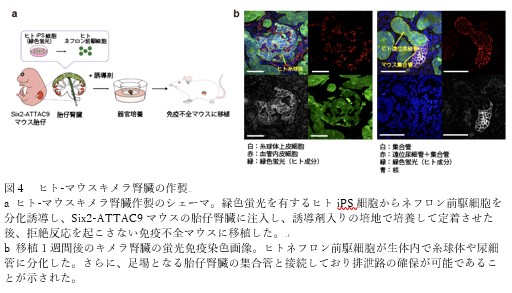
3.異種移植・再生医療研究への貢献
Six2-ATTAC9マウスの胎仔腎臓からネフロン前駆細胞を除去し、ヒトiPS細胞由来の前駆細胞を注入することで、ヒト腎組織を組み込んだキメラ腎臓の作製に成功しました。このキメラ腎臓はマウス生体内での成熟も示しました(図4)。キメラ腎臓は、異種臓器において同種であるヒトの成分を増やすことで拒絶反応を低減することが期待されており、異種移植と再生医療の融合として新たな可能性をもたらします。
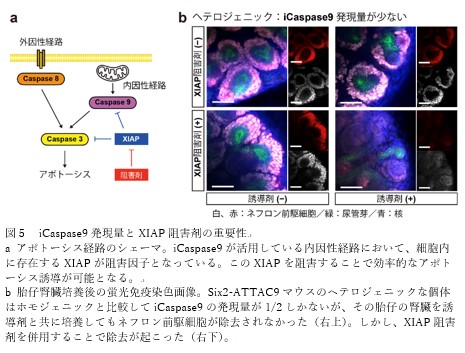
4.iCaspase9発現量とXIAP阻害剤の重要性の解明
今回の研究は、iCaspase9 の発現量がアポトーシス誘導に重要であること、また固形臓器は細胞がばらばらになった状態と比較してアポトーシスに抵抗性を示すことを、動物モデルを用いて初めて明らかにしました。さらに今回、iCaspase9 発現量が少ない場合や、アポトーシス抵抗性が高い状態であっても、アポトーシス阻害作用を持つXIAPの阻害剤を併用することでアポトーシスが誘導可能となることも明らかにしました(図5)。この発見は、これまでiCaspase9を持つ動物モデルが成功していなかった理由の一部を説明する可能性があり、本システムの応用範囲を拡大する上で重要な知見となると考えられます。
【今後の展望】
本研究成果は、CKD研究・異種移植・再生医療研究といった広範な分野にブレークスルーをもたらす可能性を秘めています。さらに、人工的アポトーシス誘導は細胞除去に伴う周囲の炎症反応が少ないという特徴から、老化細胞除去による疾患治療や健康寿命の延伸を目指す老化研究においても、ATTAC9モデルのようなアポトーシス誘導技術が有用なツールとなることが期待されます。
今後は、ATTAC9モデルを基盤として、
・CKDの進行を抑制する新たな治療法の開発
・糸球体過剰濾過のメカニズム解明
・先天性腎不全(ポッター症候群など)に対する新規治療戦略の開発
・移植可能なキメラ腎臓作製技術の確立
・ATTAC9モデルの応用範囲拡大に向けた研究
などを重点的に推進し、研究を飛躍的に発展させていく予定です。
本研究成果が、CKD、先天性腎不全に苦しむ患者さんの福音となり、異種移植・再生医療による臓器移植医療の発展、ひいては健康長寿社会の実現に貢献できるよう、研究チーム一同、総力を結集し、邁進してまいります。
【論文情報】
掲載誌: Nature Communications
論文タイトル: Caspase 9-induced apoptosis enables efficient fetal cell ablation and disease modeling (Caspase 9 誘導性アポトーシスは、効率的な胎仔細胞除去と疾患モデル作製を可能にする)
著者: Kenji Matsui, Masahito Watanabe, Shutaro Yamamoto, Shiho Kawagoe, Takumi Ikeda, Hinari Ohashi, Takafumi Kuroda, Nagisa Koda, Keita Morimoto, Yoshitaka Kinoshita, Yuka Inage, Yatsumu Saito, Shohei Fukunaga, Toshinari Fujimoto, Susumu Tajiri, Kei Matsumoto, Eiji Kobayashi, Takashi Yokoo and Shuichiro Yamanaka
DOI: 10.1038/s41467-025-57795-6
【研究グループ】
東京慈恵会医科大学 腎臓・高血圧内科
【研究費】
本研究は、以下の研究助成を受けて行われました。
・日本医療研究開発機構(AMED)
再生・細胞医療・遺伝子治療実現加速化プログラム 再生・細胞医療・遺伝子治療研究開発課題(基礎応用研究課題)「臓器再生早期実現に向けた誘導前駆細胞による胎仔キメラ作製とマルチキメラ腎臓の開発」(JP23bm1123036)
・国立研究開発法人科学技術振興機構(JST)創発的研究支援事業(JPMJFR2011)
・日本学術振興会 科学研究費助成事業(JSPS KAKENHI)
・Kidney Research Initiative-Japan: Japan Kidney Association and Nippon Boehringer Ingelheim Joint Research Project
・Eli Lilly Japan innovation research grants 2023
【用語解説】
• ATTAC9 (Apoptosis Through Targeted Activation of Caspase9)システム: 独自の人工的な細胞死誘導システム。人工的に作製された誘導剤と結合するiCaspase9を細胞に組み込み、誘導剤投与によって内因性アポトーシス経路を活性化することで、アポトーシスを誘導する。
• アポトーシス: プログラムされた細胞死。個体にとって不要になった細胞や、DNAに損傷を受けた細胞などが、周囲に炎症を起こすことなく、静かに除去される現象。内因性アポトーシス経路においては、細胞内のストレスやDNA損傷などを契機にミトコンドリアから放出されるシトクロムCを介してCaspase 9が活性化し、下流のエフェクターCaspaseを活性化してアポトーシスを実行する。
• 異種移植: 異なる種の動物間で臓器や組織を移植すること。近年ブタ臓器をヒトへの移植に活用するための研究が進んでいる。
• XIAP阻害剤: X-linked Inhibitor of Apoptosis Protein (XIAP) というタンパク質の機能を阻害する薬剤。XIAP はアポトーシスを抑制する働きを持つため、その阻害剤はアポトーシスを促進する効果が期待される。
• キメラ腎臓: 異なる種の動物の細胞を混ぜ合わせて作られた腎臓。
• 再生医療: 幹細胞や細胞加工技術などを用いて、病気や怪我で失われた体の機能回復を目指す医療。
• 糸球体: 腎臓の中にある血液を濾過するフィルターのような組織。
• 糸球体過剰濾過: 残された腎機能で老廃物を濾過しようとして、糸球体に過剰な負担がかかる状態。CKDの進行を促進する要因の一つと考えられている。
• 腎不全: 腎臓の機能が著しく低下し、老廃物を体外に排出できなくなった状態。
• 前駆細胞: 特定の組織や臓器になる前の、未分化な細胞。
• ネフロン: 腎臓の基本的な構造単位であり、血液を濾過し、尿を生成する役割を持つ機能的な構造。ヒトの腎臓には約100万個のネフロンが存在し、それぞれが独立して機能しながら、腎臓全体として体内の恒常性を維持している。
• 慢性腎臓病(CKD): 腎臓の機能が慢性的に低下していく病気の総称。進行すると腎不全となり、透析や腎移植が必要となる。
• 老化細胞: 増殖を停止した細胞。炎症性物質を分泌し、周囲の組織に悪影響を与えることが知られている。
【注釈】
注1:日本慢性腎臓病対策協議会(J-CKDI)https://j-ka.or.jp/ckd/
注2:https://www.nature.com/articles/d41586-024-01152-y, https://www3.nhk.or.jp/shutoken-news/20241003/1000109664.html
(2025/03/18 12:04)
2025/06/23 17:55
ISHA 2025へようこそ!
ISHA – 国際股関節保存学会は、2025年10月2日から4日まで、日本の…
2025/06/06 12:24
第14回日本認知症予防学会学術集会
この度、第14回日本認知症予防学会学術集会の大会長を拝命いたしま…