2025/06/06 12:24
第14回日本認知症予防学会学術集会
この度、第14回日本認知症予防学会学術集会の大会長を拝命いたしま…


医師や病気・症状、ニュースなどが検索できます
【研究成果の概要】
近年、腸内細菌とアルツハイマー病が密接に関連していることが明らかになっています。ヒトならびにアルツハイマー病モデルマウスを用いた研究では、腸内細菌の組成(腸内細菌叢)の変化が認知機能に影響することが報告されています。また、いくつかのプロバイオティクス(下記*参照)をアルツハイマー病モデルマウスに摂取させると認知機能の改善が見られますが、プロバイオティクスが認知機能やアミロイドβタンパク質(Aβ)沈着・産生、グリア細胞の活性化などに影響する分子メカニズムは不明であります。
今回、名古屋市立大学大学院医学研究科神経生化学分野の道川 誠教授、鄭 且均准教授は、ビフィズス菌MCC1274 をアルツハイマー病モデルマウスに摂取させると、アルツハイマー病モデルマウスで見られる記憶障害が予防されることを明らかにしました。そのメカニズムとしては、ビフィズス菌MCC1274 はAβ 産生や沈着を低下させ、海馬でのミクログリアの活性化を抑制し、その結果炎症性サイトカイン産生を低下させることで記憶障害を予防することを見いだしました。
本研究はアルツハイマー病研究の専門誌である「Journal of Alzheimer’s Disease」 に令和 3年 12月 21日にPer-pressとして公開されました。
*「乳酸菌やビフィズス菌など、一定量を摂取したときに宿主に有益な影響を与える生きた微生物」
【研究の背景と目的】
アルツハイマー病は、超高齢社会に突入した、わが国において増加する認知症の半数以上を占める神経変性疾患であり、65 歳以降に発症率が増加する疾患です。20 年以上かけて脳内にゆっくりとAβ が凝集した老人斑が脳内に沈着し、その後タウタンパク質の凝集した神経原線維変化が神経細胞内に形成されるに伴って認知機能障害が引き起こされると考えられています。このとき、脳内では神経細胞やシナプスの減少に加えて、グリア細胞の活性化、炎症などが見られ、これらが相まって認知機能障害を引き起こしていると考えられます。従ってアルツハイマー病発症前の長い期間において、もしAβ の産生ならびにアミロイド沈着を抑制し、アミロイド沈着によって引き起こされる炎症を抑制するような生活習慣や食事などのアルツハイマー病を予防する因子が明らかになれば、真に有効な予防法となる可能性があります。
これまでに、ビフィズス菌 MCC1274について、軽度認知障害が疑われる方 を対象 と した臨床試験において顕著な認知機能改善作用が 確認されました。本研究では、ビフィズス菌 MCC1274の作用メカニズムの解明ならびに医薬品用途の可能性を探索するために、アルツハイマー病モデルマウスを用いて研究を行いました。
【研究の成果】
私たちは、今回の研究によって、ビフィズス菌MCC1274(Bifidobacterium breve MCC1274) をアルツハイマー病モデルマウスに経口摂取させたところ、脳内のアルツハイマー病病態の発症・進行が抑制され、記憶障害を予防することを明らかにしました。すなわち、①「ビフィズス菌MCC1274」経口投与群では、記憶障害が予防され(図1)、②海馬でのAβ 沈着やAβ 産生が有意に低下しました(図2)。しかし大脳皮質ではAβ 沈着やAβ 産生の低下は見られませんでした。「ビフィズス菌MCC1274」によるAβ レベルの低下メカニズムを明らかにするため、Aβ 産生に関わるアミロイド前駆タンパク質(APP)切断酵素の発現を検討した結果、③「ビフィズス菌MCC1274」投与群ではAβ 産生を抑制する酵素である
ADAM10(α-secretase)の発現が増加することが分かりました。④ADAM10 発現を増加させるメカニズムとしては、ビフィズス菌MCC1274 はPKC やERK を活性化させることでその下流にあるHIF-1αおよびCREB タンパク質の発現を増加させることがわかりました。さらに、⑤「ビフィズス菌MCC1274」投与群の海馬ではミクログリアのマーカーであるIba1 陽性細胞数が減少し(図3A と3B)、それによって炎症性サイトカインの産生も低下することが明らかになりました(図3C と3D)。以上をまとめると、「ビフィズス菌MCC1274」は、Aβ 産生と脳内炎症を抑制することによってアルツハイマー病モデルマウスで見られる記憶障害を予防すると考えられます(図1)。
【研究のポイント】
ビフィズス菌MCC1274 をアルツハイマー病モデルマウスに経口投与すると、
・記憶障害を予防しました。
・海馬でのAβ 沈着やAβ 産生が有意に低下しました。
・海馬でのミクログリアの活性化を抑制し炎症性サイトカインの産生が低下しました。
【研究の意義と今後の展開や社会的意義など】
以上の結果は、ビフィズス菌MCC1274 を摂取することでアルツハイマー病発症を抑制できる可能性をアルツハイマー病モデルマウスを使った研究で示したものであり、ビフィズス菌の経口摂取によってアルツハイマー病発症を予防できる可能性を示しており、社会的にも意義があると考えておりま す。現在、他の研究者による臨床試験も進行しており、ヒトにおいてもビフィズス菌MCC1274 を摂取することにより認知機能低下の予防効果があるという結果が出てきておりますので、そのメカニズムを明らかにした点でも意義があると考えております。今後は、今回明らかにした予防効果の他に、アルツハイマー病発症後の治療効果について、さらに検討を進めたいと思っております。
【用語解説】
1.アミロイド β(Aβ): アルツハイマー病病態を促進させる鍵分子である Aβは、アミロイド前駆タンパク質(APP)から二つのプロテアーゼ(βおよびγセクレターゼ)で順次切断されることにより産生される。
2.ミクログリア:脳内のグリア細胞の1種類であり、活性化することにより炎症性サイトカインを分泌し、神経細胞にダメージを与える。
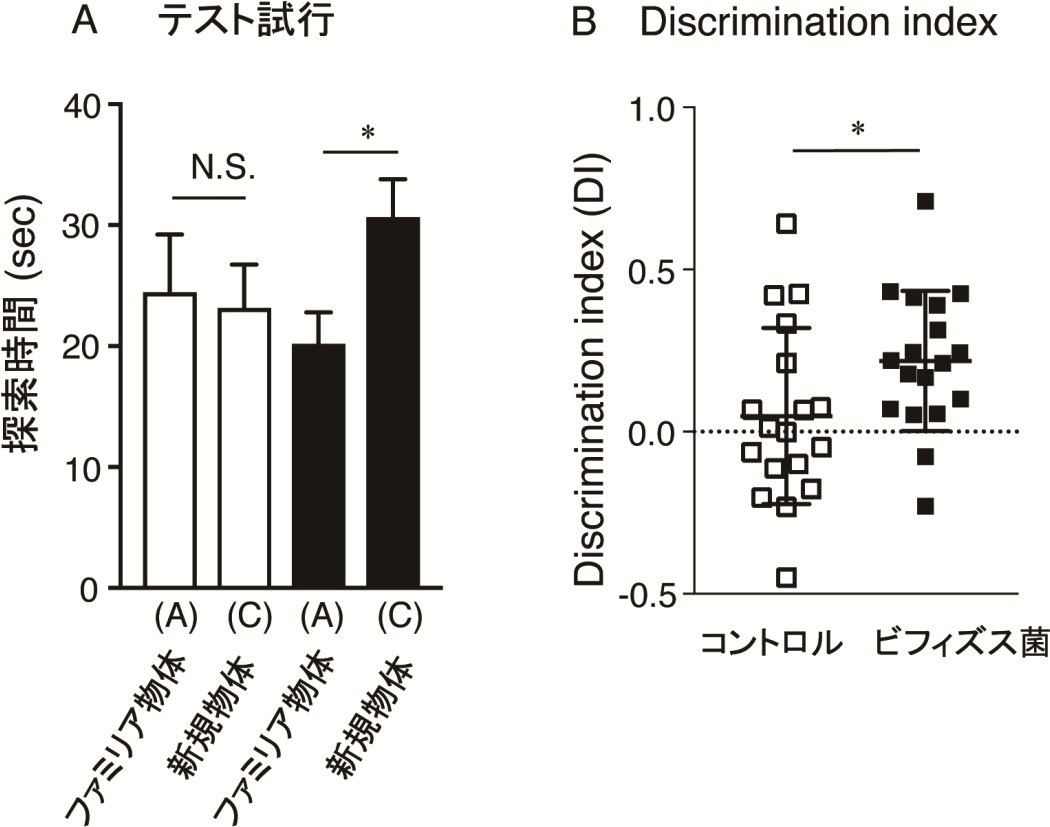
図1。ビフィズス菌MCC1274 投与は記憶障害を予防する。3カ月齢アルツハイマー病モデルマウスにビフィズス菌MCC1274 を4カ月間経口投与し、新規物体認識試験を行い、認知機能を評価した。測定用ケージに同じ形をした物体二つ(ファミリア物体)を入れ、5分間それぞれの物体に対する探索時間を計測する。24時間後一つだけ形の異なる物体(新規物体)に変えて、同様に探索時間を計測する(A)。それぞれの物体に対する探索時間の割合(新規物体探索時間/ファミリア物体探索時間+新規物体探索時間)を”Discrimination index”として評価する(B)。
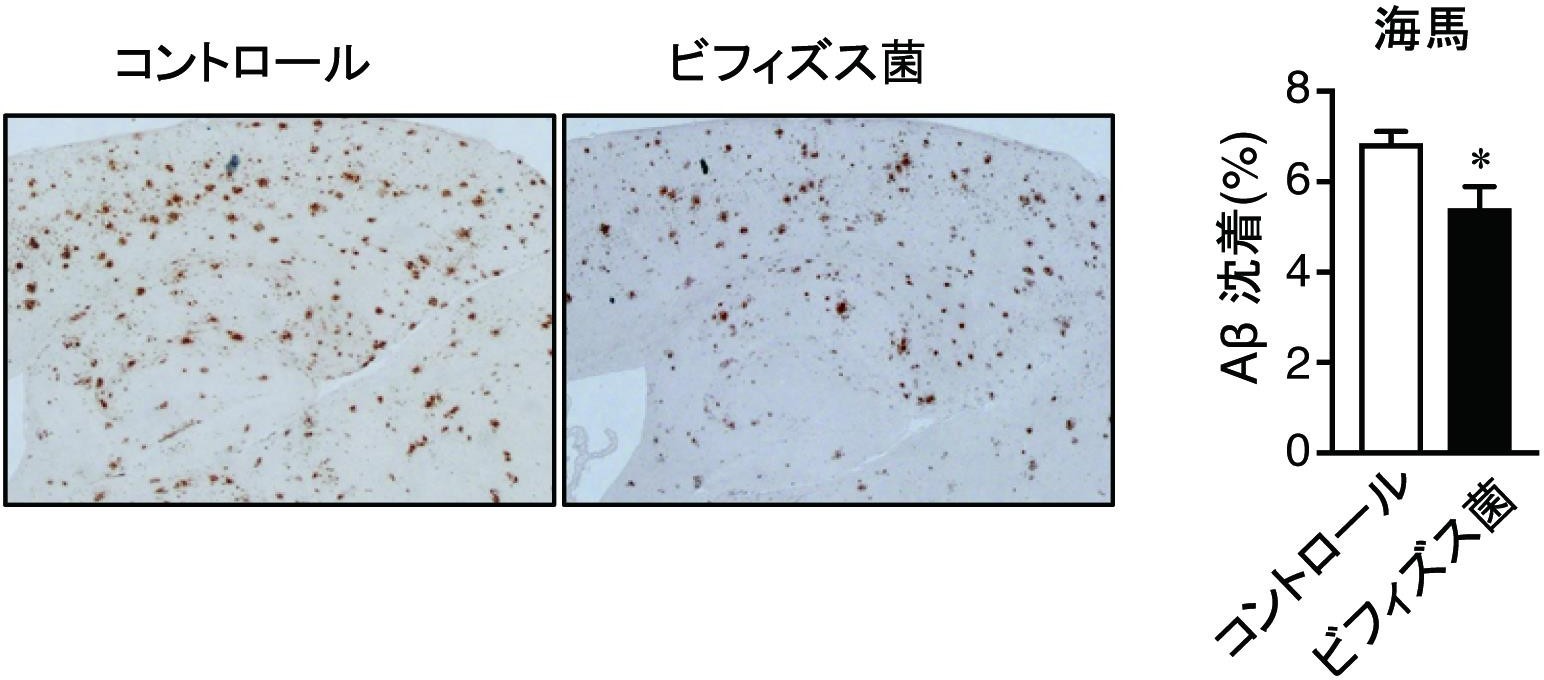
図2。ビフィズス菌MCC1274投与は脳内Aβ沈着を低下する。3カ月齢アルツハイマー病モデルマウスにビフィズス菌MCC1274 を4カ月間経口投与し、脳切片を用いてAβ 抗体で染色した
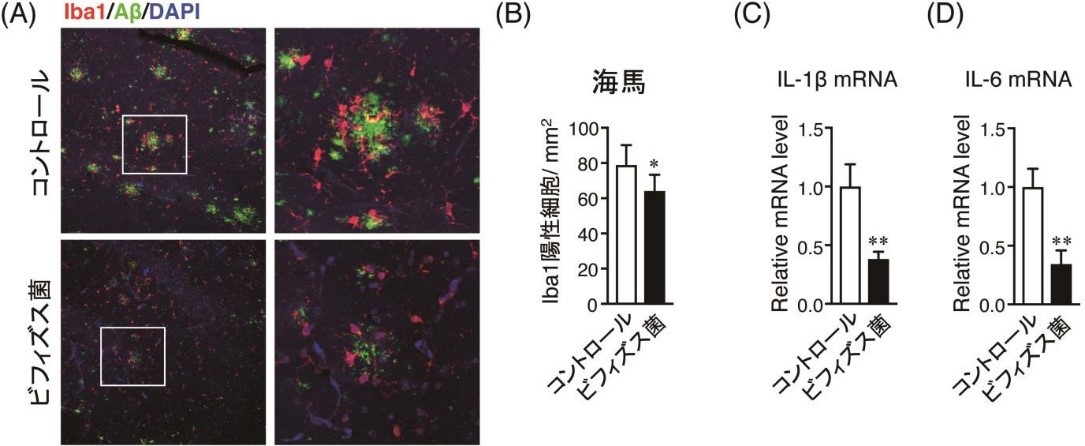
図3。ビフィズス菌MCC1274 投与はミクログリアの活性化を抑制し炎症性サイトカイン産生が低下する。3カ月齢アルツハイマー病モデルマウスにビフィズス菌MCC1274 を4カ月間経口投与し、脳切片を用いてAβ 抗体とIba1 抗体(ミクログリアマーカー)で染色した(A)。Iba1 陽性細胞の定量化(B)。炎症性サイトカインであるIL-1β(C)とIL-6(D)のmRNA の発現。
【研究助成】
本研究は、JSPS 科研費 JP16H05599、JP15K15712、JP20K07762 の助成を受けたものです。
【論文タイトル】
Probiotic Bifidobacterium breve prevents memory impairment through the reduction of both Aβ production and microglia activation in APP knock-in mouse
(アルツハイマー病モデルマウスにおいてビフィズス菌MCC1274 の経口投与は、Aβ 産生とミクログリアの活性化を低下させることで記憶障害を防ぐ)。
【著者】
Mona Abdelhamid1, Chunyu Zhou1, Kazuya Ohno2, Tetsuya Kuhara2, Ferdous Taslima1, Mohammad Abdullah1, 3, Cha-Gyun Jung1, * and Makoto Michikawa1, *
Mona Abdelhamid1, 周 春雨1, 大野和也2, 久原徹哉2, Ferdous Taslima1, Mohammad Abdullah1, 3, 鄭 且均1, *, 道川 誠1, *(*責任著者)
【所属】
1名古屋市立大学大学院医学研究科神経生化学分野2森永乳業(株) 基礎研究所
3 Department of Neuroscience, Mayo Clinic, Jacksonville, Florida, USA.
【掲載学術誌】
学術誌名;Journal of Alzheimer’s Disease
DOI 番号:10.3233/JAD-215025
【ビフィズス菌MCC1274に関する既往研究論文】
Probiotic Bifidobacterium breve in improving cognitive functions of older adults with suspected mild cognitive impairment: a randomized, double-blind, placebo-controlled trial(軽度認知障害が疑われる方における認知機能改善作用),Journal of Alzheimer’s Disease 2020;77(1):139-147.
【研究に関する問い合わせ】
(1)名古屋市立大学大学院医学研究科 教授 道川 誠
住所:〒467-8601 名古屋市瑞穂区瑞穂町字川澄1
E-mail:michi@med.nagoya-cu.ac.jp
(2)名古屋市立大学大学院医学研究科 准教授 鄭 且均
住所:〒467-8601 名古屋市瑞穂区瑞穂町字川澄1
E-mail:jung@med.nagoya-cu.ac.jp
【報道に関する問い合わせ】
名古屋市立大学 医学・病院管理部経営課 住所:名古屋市瑞穂区瑞穂町字川澄1
TEL:052-858-7114 FAX:052-853-7537
E-mail:hpkouhou@sec.nagoya-cu.ac.jp
連携できる企業様でご関心をお持ちいただける場合のご連絡につきましては、下記の問い合わせ先にて承ります。
【産学連携・共同研究等に関する問い合わせ】
名古屋市立大学 事務局大学管理部学術課
住所:名古屋市瑞穂区瑞穂町字川澄1
TEL:052-853-8309 FAX:052-841-0261
E-mail:ncu-innovation[at]sec.nagoya-cu.ac.jp
(2022/01/20 11:35)
2025/06/06 12:24
第14回日本認知症予防学会学術集会
この度、第14回日本認知症予防学会学術集会の大会長を拝命いたしま…
2025/06/03 11:41
口腔がんの診断数、著名人のがん公表後に約1.5倍に
Oral disease、2025年5月15日研究成果の概要 公立大学法人名古屋市…
2025/06/02 10:57
治療タンパク質を脳へ輸送する新たな遺伝子治療法を開発
東京慈恵会医科大学遺伝子治療研究部の松島小貴、小林博司、医学部…