2025/06/06 12:24
第14回日本認知症予防学会学術集会
この度、第14回日本認知症予防学会学術集会の大会長を拝命いたしま…


医師や病気・症状、ニュースなどが検索できます
◇概要
生体が恒常性を維持するためには、不要あるいは合成不良のタンパク質が適切に分解処理されなければならない。このタンパク質の分解処理に関わるタンパク質複合体(プロテアソーム)を構成するサブユニットタンパク質の遺伝子バリアント(遺伝子の違い)により、難治性の慢性炎症疾患(プロテアソーム関連自己炎症症候群)が発症する。今回、和歌山県立医科大学先端医学研究所改正恒康、邊見弘明(現在岡山理科大学獣医学部)、同大学皮膚科学金澤伸雄(現在兵庫医科大学皮膚科学)、琉球大学小児科金城紀子、岐阜大学医学系研究科小児科学分野大西秀典、長崎大学原爆後障害医療研究所吉浦孝一郎、東京大学大学院薬学系研究科村田茂穂、兵庫県立大学大学院理学研究科水島恒裕らの研究グループは、プロテアソームサブユニットβ1iをコードする遺伝子(PSMB9)のde novo(注1)の新規のヘテロ接合性アミノ酸置換バリアントにより、免疫不全を伴うプロテアソーム関連自己炎症症候群という新たなタイプの遺伝性疾患が生じることを見いだし、その病態を再現する新規のモデルマウスを樹立した。
プロテアソームの機能障害を来す新たな疾患概念が提起され、そのモデルマウスが得られたことから、今後、プロテアソームの機能異常による病態の解明が進み、プロテアソーム関連自己炎症症候群、免疫不全などを制御する新たな治療法の開発が進むことが期待される。
本研究成果は2021年11月24日(米国時間)に、国際誌Nature Communicationsに発表された。
1. 背景
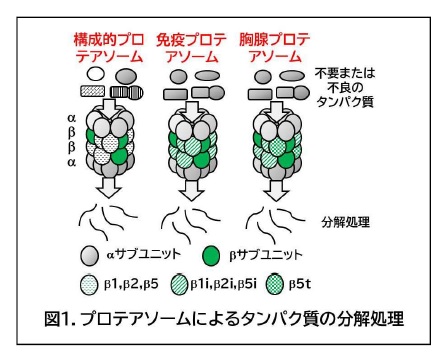
プロテアソームは、不要になったり、うまく合成されなかったりしたタンパク質を分解処理することにより、細胞、組織の恒常性維持に必須の役割を果たすタンパク質複合体であり、7個のαサブユニット(α1-7)、7個のβサブユニット(β1-7)がリング状に結合することにより構成されている(図1、注2)。近年、これらのサブユニットをコードする遺伝子のバリアントが、周期性の発熱、皮疹、進行性の脂肪筋肉萎縮を来し、自己炎症性疾患(注3)の原因となることが明らかとなり、プロテアソーム関連自己炎症症候群(Proteasome-associated autoinflammatory syndrome、PRAAS)(注4)と総称されている。PRAASの病態については、炎症性サイトカインであるIL-6やI型インターフェロンの過剰産生などが生じていることが指摘されているが、適切なモデルマウスがなく、プロテアソームの機能障害によりどのような機構で病態が生じるのかについてはほとんど不明であり、有効な治療法も確立されていない。
2. 研究成果
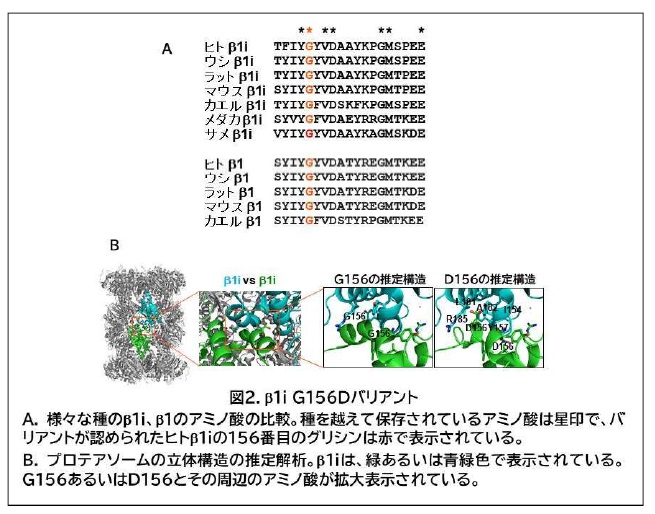
周期性かつ難治性のPRAAS様の炎症症状を新生児期に発症しながらも、通常のPRAASに認められる脂肪萎縮を示さず、また、PRAASではほとんど認められない肺高血圧やリンパ球減少(獲得免疫不全)を示す独立した2症例(琉球大学小児科、岐阜大学小児科)が見つかった。そして、詳細な遺伝子解析により、どちらの患者においても、プロテアソームサブユニットβ1iをコードする遺伝子(PSMB9)にde novoの新規のヘテロ接合性バリアント(β1iの156番目のアミノ酸であるグリシンをアスパラギン酸に置換させるバリアント、G156D)が病態の原因として有力な候補であることが示唆された。また、立体構造の推定解析により、この遺伝子バリアントがプロテアソームの構造に障害を来すことも示された(図2)。さらに、患者由来の細胞を解析したところ、β1iのタンパク質が十分成熟せず、プロテアソームの構造および機能が障害されていた。
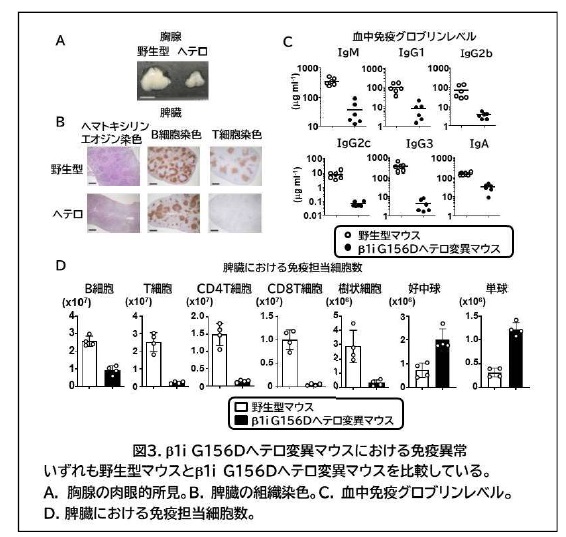
次に、G156Dの病理的意義を明らかにするため、CRISPR/Cas9法(注5)により、G156D変異をマウスに導入し解析したところ、G156Dヘテロ変異マウスにおいて、患者由来の細胞での所見と同様のパターンで、β1iタンパク質の成熟、プロテアソームの構造および機能が障害されていた。また、G156Dヘテロ変異マウスを免疫学的に解析したところ、獲得免疫については、胸腺が萎縮する(図3A)と共に、脾臓(ひぞう)ではT細胞とB細胞いずれのリンパ球も減少し(図3B)、抗体(免疫グロブリン)産生も顕著に低下しており(図3C)、自然免疫については、樹状細胞が減少している一方で、好中球や単球は増加していた(図3D)。G156Dヘテロ変異マウスに認められたプロテアソーム障害、免疫異常の表現型は、同変異を有する患者の所見と共通する部分が多く、G156D変異が患者の病態の原因であることが強く示唆された。
3. 結論および波及効果
以上のように、新生児期に免疫不全を伴う自己炎症性疾患を発症した独立した日本人患者2症例に共通して、プロテアソームサブユニットβ1iのアミノ酸置換を来す、新規のヘテロ接合性遺伝子バリアント(G156D)が病態の原因であることを見いだした。このバリアントは、これまでのPRAASと異なり、単一遺伝子のヘテロ接合性バリアント、すなわち常染色体顕性(優性)遺伝様式である点がユニークであると言える(注6)。また、これまでのPRAASの原因となる遺伝子バリアントは、主に、プロテアソームのタンパク質分解酵素の活性中心の構造に影響を及ぼし、構造異常と共に顕著な活性低下を来すのに対し、β1i G156Dバリアントでは、プロテアソームのリング構造への影響が主で、タンパク質分解酵素の活性中心の構造は保持され、プロテアソーム活性は障害されているもののユビキチンの蓄積がほとんど見られないという特徴を有する。さらに、臨床所見においても、これまでのPRAASと比較して、脂肪萎縮を示さず、肺高血圧が顕著で、獲得免疫不全が認められるなどの相違点が認められる。以上の点から、今回同定されたβ1i G156Dバリアントは、PRAASと似て非なる病態を引き起こしている可能性が強く示唆され、われわれは、免疫不全を伴う自己炎症性疾患(PRAAS with immunodeficiency、PRAAS-ID)という新規の疾患概念を提唱する。
また、これまでPRAASの病態を再現するモデルマウスは報告されていないが、本研究で樹立したβ1i G156D変異マウスでは、プロテアソームの障害パターン、免疫異常など、患者の所見を再現することができた。プロテアソームの機能異常は老化、神経変性疾患、難治性腸炎、がんなどさまざまな病態にも認められる。β1i G156D 変異マウスの解析を進めることにより、プロテアソーム関連自己炎症症候群、免疫不全に加えて、プロテアソームの機能異常を来すさまざまな病態のメカニズムが解明され、新たな制御手段、治療法の開発が進むことが期待される。
4. 掲載論文
掲載誌:Nature Communications
題目:Heterozygous missense variant of the proteasome subunit β-type 9 causes neonatal-onset autoinflammation and immunodeficiency.
著者:Kanazawa N, Hemmi H, Kinjo N, Ohnishi H, Hamazaki J, Mishima H, Kinoshita A, Mizushima T, Hamada S, Hamada K, Kawamoto N, Kadowaki S, Honda Y, Izawa K, Nishikomori R, Tsumura M, Yamashita Y, Tamura S, Orimo T, Ozasa T, Kato T, Sasaki I, Fukuda-Ohta Y, Wakaki-Nishiyama N, Inaba Y, Kunimoto K, Okada S, Taketani T, Nakanishi K, Murata S, Yoshiura K, Kaisho T.
URL: https://doi.org/10.1038/s41467-021-27085-y
5. 補足説明
注1 de novo:ここでは、親から受け継いだ遺伝子バリアントではなく、患者に新たに生じた遺伝子バリアントであることを示す。
注2 プロテアソーム:真核生物のすべての細胞に、構成的プロテアソーム、免疫プロテアソーム、胸腺プロテアソームのいずれかの形で存在している。構成的プロテアソームでは、タンパク質分解活性を担うサブユニットとして、β1、β2、β5が含まれているが、免疫プロテアソームでは、β1i、β2i、β5i、胸腺プロテアソームでは、β1i、β2i、β5tが含まれている。タンパク質が分解される際には、76個のアミノ酸から構成されるユビキチンが付加されるので、プロテアソームの機能低下により、細胞や組織にユビキチンが蓄積する。
注3 自己炎症性疾患:好中球やマクロファージなど自然免疫系の過剰な活性化により、難治性の非感染性炎症を来す疾患の総称。多くは遺伝性で、家族性地中海熱、クリオピリン関連周期熱症候群、プロテアソーム関連自己炎症症候群などが含まれる。
注4 プロテアソーム関連自己炎症症候群(PRAAS):プロテアソームを構成するタンパク質の遺伝子バリアントを原因とする自己炎症性疾患の総称。1930年代から本邦で報告され、報告者である東北帝国大学皮膚科教授中條敦、和歌山県立医科大学皮膚科教授西村長應の名前を冠する、指定難病の中條・西村症候群はその一つであり、2011年に和歌山県立医科大学金澤、長崎大学吉浦、徳島大学安友らによって、プロテアソームサブユニットβ5iをコードする遺伝子(PSMB8)のホモ接合性バリアントを原因とする常染色体潜性(劣性)遺伝性疾患であることが明らかになっている。相前後して海外からも、β5iおよびそれ以外のプロテアソームサブユニットをコードする遺伝子のバリアントを原因とする症例が報告されている。
注5 CRISPR/Cas9:clustered regularly interspaced short palindromic repeat-Cas9の略。DNA二本鎖を切断してゲノム配列の任意の場所を削除、置換、挿入することができる遺伝子改変技術である。開発者は2020年にノーベル化学賞を受賞している。
注6 これまでに報告されてきたPRAASの原因となるプロテアソームサブユニット遺伝子のバリアントは、両染色体に単一遺伝子のバリアント(ホモ接合性バリアントすなわち同じバリアントか、あるいは、複合ヘテロ接合性バリアントすなわち異なるバリアント)が検出される常染色体潜性(劣性)遺伝様式か、あるいは両染色体にそれぞれ異なる二つの遺伝子のバリアント(2遺伝子ヘテロ接合性バリアント)が検出される遺伝様式をとっている。
記者会見のお知らせ
本件に関して、12月6日(月)16時から和歌山県立医科大学 紀三井寺キャンパス 附属病院
東棟3階 地域医療支援センターにて記者会見を行います。ぜひともご取材のほど、よろしくお願い申し上げます。
【日 時】 2021年12月6日(月) 16:00~16:45
【発表者】 兵庫医科大学 皮膚科学 教授 金澤 伸雄
和歌山県立医科大学 先端医学研究所 生体調節機構研究部 教授 改正 恒康
【会場】 和歌山県立医科大学 紀三井寺キャンパス 附属病院東棟3階 地域医療支援センター
(2021/12/03 08:22)
2025/06/06 12:24
第14回日本認知症予防学会学術集会
この度、第14回日本認知症予防学会学術集会の大会長を拝命いたしま…
2025/06/03 11:41
口腔がんの診断数、著名人のがん公表後に約1.5倍に
Oral disease、2025年5月15日研究成果の概要 公立大学法人名古屋市…
2025/06/02 10:57
治療タンパク質を脳へ輸送する新たな遺伝子治療法を開発
東京慈恵会医科大学遺伝子治療研究部の松島小貴、小林博司、医学部…