2025/06/23 17:55
ISHA 2025へようこそ!
ISHA – 国際股関節保存学会は、2025年10月2日から4日まで、日本の…
発表のポイント
• がんゲノムデータベースに登録される約7万種類の遺伝子変異のコンピューター解析により、RETがん遺伝子に新たな治療標的となる遺伝子変異があることを発見しました。
• がんゲノム医療の現場で同定される意義の不明な遺伝子変異の中には、既存の抗がん剤の治療効果が見込まれる治療標的変異が含まれていることが示されました。
• さまざまな遺伝子の意義不明変異を意義付けすることで、がんゲノム医療による患者さんの治療機会が拡大することが期待されます。
概要
学校法人慈恵大学(理事長:栗原 敏、東京都港区)、国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区)、国立大学法人京都大学(総長:湊 長博、京都市左京区)、国立大学法人筑波大学(学長:永田 恭介、茨城県つくば市)などからなる研究チームは、がんゲノムデータベースに登録される約7万種類の遺伝子変異に対するコンピューター解析やそれに基づく細胞実験を行い、これまで薬剤の有効性が確認できておらず意義が不明とされていた変異のなかから既存薬剤のRET阻害薬による治療効果が見込まれる新たなRET遺伝子の変異を発見しました。RET遺伝子の変異は、甲状腺がんをはじめとして幅広いがんに見られますが、RET阻害薬の有効性を確認できているのは特定の変異を有する一部の患者さんで、意義が不明の変異を有する患者さんにおいての有効性はその多くが解明されていませんでした。
がんゲノム医療の現場では、RET遺伝子に限らず、さまざまな遺伝子で意義の不明な遺伝子変異が頻繁に見つかります。本研究により意義の不明な遺伝子変異の中には、既存の抗がん剤の治療効果が見込まれる治療標的変異が含まれていることが示され、今後、コンピューター解析によりこれらの変異の意義を推定していくことにより、患者さんの抗がん剤による治療機会が拡大することが期待されます。
本研究は、東京慈恵会医科大学産婦人科学講座 田畑潤哉医員、岡本愛光教授、国立がん研究センター研究所ゲノム生物学研究分野 中奥敬史主任研究員、河野隆志分野長、京都大学大学院医学研究科 荒木望嗣特定准教授、奥野恭史教授、筑波大学医学医療系 吉野龍ノ介助教、東北大学加齢医学研究所 宇井彩子准教授、東京工業大学 情報理工学院 情報工学系 関嶋政和准教授らからなる研究チームにより行われたもので、研究成果は科学誌「Cancer Research」に9月27日に掲載されます。
背景
がん細胞に生じた遺伝子変異を見つけ出し、変異に有効な抗がん薬を投与するがんゲノム医療 (注1) が全国のがんゲノム医療中核拠点・拠点・連携病院で保険診療として行われています。しかし、患者さんでみられる遺伝子変異の多くは発がんや治療における意義がわからない意義不明変異(VUS, variants of unknown significance) (注2)です。これらの変異は検出されたとしても、効果の見込まれる抗がん薬が見いだせず、がんゲノム医療における大きな課題となっています。今後、がんゲノム医療をより有用なものとするためには、この意義不明変異の意義を理解し、治療に生かしていくことが必要です。
RET遺伝子 (注3) は、他の遺伝子との融合や変異によって活性化し、肺がんや甲状腺がんを引き起こすがん遺伝子です。これらの遺伝子変化を持つがんに対し高い効果を持つ治療薬としてRET阻害剤が開発され、保険診療で用いられています。しかし、RET遺伝子の変異については、RET阻害剤が投与される対象となるのは、有効性が確認できているホットスポット変異と呼ばれる一部の変異のみで、他の多くは意義不明変異とされてきました。
研究内容
本研究では、さまざまながんで見られる変異を集めたデータベース (注4) であるGENIEデータベース (https://www.aacr.org/professionals/research/aacr-project-genie/) に登録される7万個以上の遺伝子変異に対して、コンピューターを用いるインシリコ技術によりがんの進化の過程での正の選択やタンパク質の可動性への影響を推定しました。その結果、RET遺伝子の意義不明変異の中に、治療標的となる新たな変異群が存在することを発見しました。
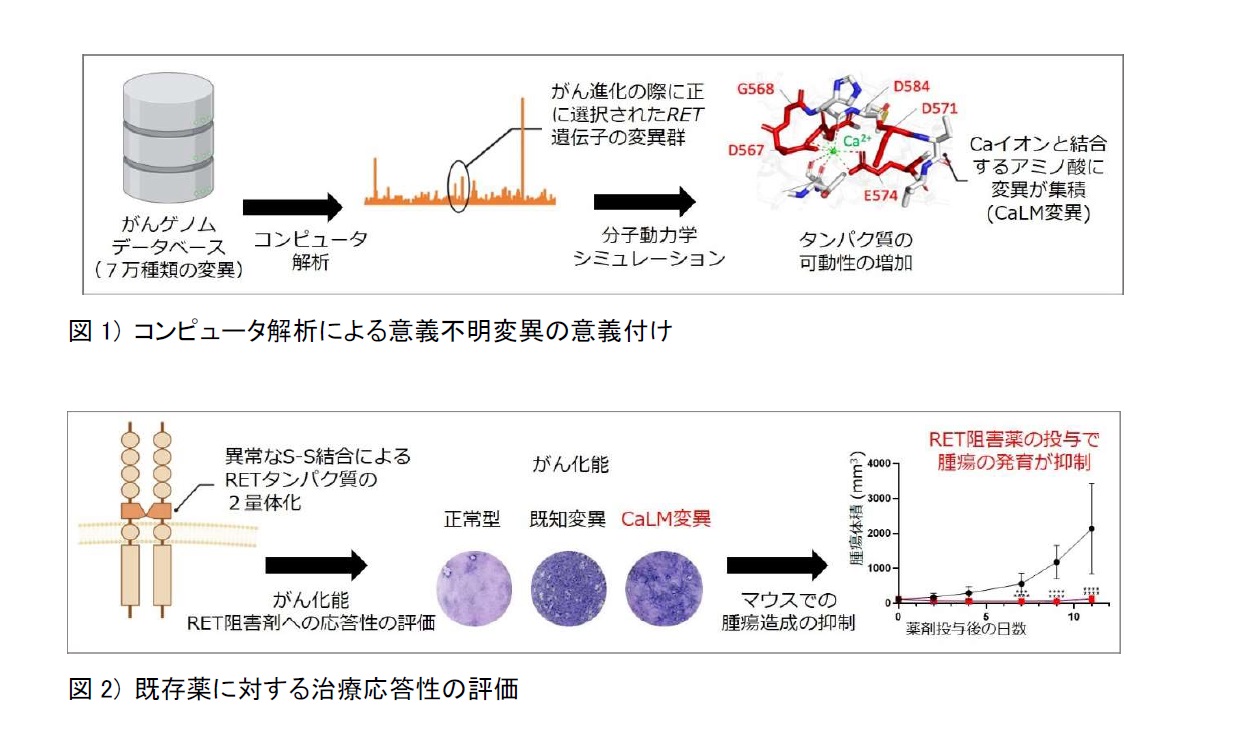
この変異は、RET遺伝子のCaイオン結合モチーフ (CaLM, カルモジュリン様モチーフ) に存在し、肺がん、大腸がん、乳がんなど複数のがんで見られました。「富岳」「TSUBAME3.0」など複数のスーパーコンピューターを用いた分子動力学シミュレーション (注5)から、このCaLM変異はRETタンパク質とCaイオンの結合を低下し、RETタンパク質の可動性を高めるなど大きな影響を持つことが推定されました(図1)。細胞や精製したタンパク質の実験を行ったところ、シミュレーションでの推定と合致して、RET変異タンパク質は異常な共有結合により二量体化し、RETタンパク質の持つキナーゼ酵素の恒常的な活性化を引き起こし、細胞をがん化させるなど、RETタンパク質の機能を大きく変化させることが分かりました (図2) 。
また、このRET変異タンパク質の恒常的な活性化や変異腫瘍細胞の増殖は、セルペルカチニブ、プラルセチニブという既存のRET阻害薬で抑えられました。よって、RET遺伝子のCaLM変異を持つがんには、RET阻害薬による治療が効果を示す可能性があります。
今回発見されたRET遺伝子のCaLM 変異を持つがんの患者さんに、RET阻害剤が治療効果をもたらすか、臨床試験を行うことで確認していきたいと考えます。また、RET遺伝子以外にも意義不明変異は数多く見られます。今後、本研究で用いたインシリコ解析技術を用いてさまざまな遺伝子で見つかる意義不明変異の意義を解釈することで、既存の抗がん薬による治療効果が見込まれる遺伝子変異群を見つけ出し、患者さんの治療機会を拡大できると期待します。
(2022/09/27 14:24)
2025/06/23 17:55
ISHA 2025へようこそ!
ISHA – 国際股関節保存学会は、2025年10月2日から4日まで、日本の…
2025/06/06 12:24
第14回日本認知症予防学会学術集会
この度、第14回日本認知症予防学会学術集会の大会長を拝命いたしま…