ファイザーは4月18日、今年(2024)年3月に再発または難治性の多発性骨髄腫(MM)を適応症として承認された抗BCMA/CD3二重特異性抗体エルラナタマブ(商品名エルレフィオ皮下注44mg、同76mg)に関するメディアセミナーを開催。登壇した日本赤十字社医療センター(東京都)骨髄腫アミロイドーシスセンター顧問の鈴木憲史氏は「MM患者の予後を改善するとともに、利便性の高い薬剤としても期待される」と述べた(関連記事「多発性骨髄腫に対する初の二重特異性抗体が承認」)。
ファイザーは4月18日、今年(2024)年3月に再発または難治性の多発性骨髄腫(MM)を適応症として承認された抗BCMA/CD3二重特異性抗体エルラナタマブ(商品名エルレフィオ皮下注44mg、同76mg)に関するメディアセミナーを開催。登壇した日本赤十字社医療センター(東京都)骨髄腫アミロイドーシスセンター顧問の鈴木憲史氏は「MM患者の予後を改善するとともに、利便性の高い薬剤としても期待される」と述べた(関連記事「多発性骨髄腫に対する初の二重特異性抗体が承認」)。
治療法進歩も、アンメットニーズ存在
近年、MMの治療法は大きく進歩しており、2000年代以降にプロテアソーム阻害薬、免疫調整薬、抗CD38抗体製剤が登場した他、2022年にはB細胞成熟抗原(BCMA)を標的とするキメラ抗原受容体発現T(CAR-T)細胞療法が相次いで承認されたことで、患者の予後が改善されている。
現在、自家造血幹細胞移植の適応がない初発MMに対しては、ダラツムマブ+レナリドミド+低用量デキサメタゾン(DLd)療法またはダラツムマブ+メルファラン+プレドニゾロン+ボルテゾミブ(D-MPB)療法が推奨されている。再発・難治性MMに対してはボルテゾミブやレナリドミドなどが使用される。
しかし、患者の多くは再発を繰り返し、キードラッグであるプロテアソーム阻害薬、免疫調整薬、抗CD38抗体製剤に対し抵抗性を示すことが問題となっている。
また、CAR-T細胞療法は高い有効性が認められ、昨年にはイデカブタゲン ビクルユーセルが早期から使用可能になったものの、鈴木氏は「実施施設が限られる、輸送や製造に時間がかかり、その間に増悪する可能性があるといった課題が残る」と指摘した。
ORRは61%、長期追跡調査でも良好
そのような背景の下、新たに登場したのがエルラナタマブである。同薬は骨髄腫細胞上に過剰発現するBCMAを標的とし、BCMAとT細胞上のCD3の両者に結合することで細胞傷害性サイトカインおよび細胞融解酵素の放出を誘導して腫瘍細胞を傷害する二重特異性抗体である。
エルラナタマブの有効性および安全性は、第Ⅱ相国際共同臨床試験MagnetisMM-3で検証された。同試験では、BCMAを標的とした治療がエルラナタマブによる治療に及ぼす影響を検討するため、2つの独立したコホートを設定。コホートAではBCMA標的治療歴のない患者、コホートBではBCMA標的治療歴〔抗体薬物複合体(ADC)/CAR-T細胞療法〕がある患者を対象とした。
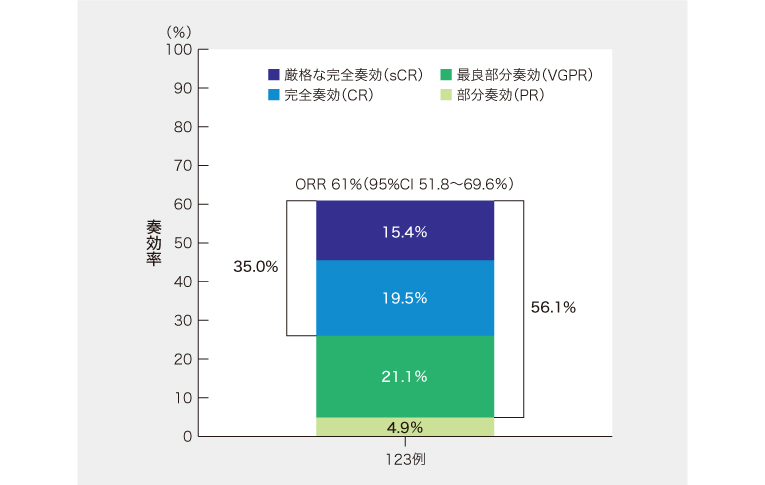
解析の結果、コホートAの追跡期間中央値14.7カ月における盲検化独立中央判定(BICR)による奏効率(ORR)は61.0%(95%CI 51.8~69.6%)と、事前に設定した閾値(30%)を上回り主要評価項目を達成した(P<0.0001、片側正確2項検定)。完全奏効(CR)以上は35.0%、最良部分奏効(VGPR)以上は56.1%だった(図)。
図. BICRによる奏効率
また、長期追跡調査(中央値15.9カ月)ではCR以上かつ微小残存病変(MRD)の評価が可能な患者の89.7%(29例)でMRD陰性を達成。奏効期間(DOR)中央値は評価不能、無増悪生存(PFS)、全生存(OS)の中央値はそれぞれ17.2カ月(95%CI 9.8カ月~評価不能)、21.9カ月(同13.4~評価不能)と良好な結果が示された。
なお、MagnetisMM-3および第Ⅰ相国内試験MagnetisMM-1など4件のMagnetisMM試験のプール解析により、BCMA標的治療歴のある患者においてもエルラタナブの有効性が示されている。
治療初期のサイトカイン放出症候群に注意
安全性については、解析対象183例のうち91.3%で有害事象が認められた。主な有害事象はサイトカイン放出症候群(CRS)が57.9%、好中球減少症が36.1%、貧血が26.8%、リンパ球減少症が23.5%、注射部位反応が21.3%だった。
エルラタナブは通常、初回に12mg、4日目に32mgを皮下投与し、8日目以降は1回76mgを1週間間隔で皮下投与する。24週間以上投与し、奏効が認められた場合は1回76mgを隔週投与とする。鈴木氏は「CRSの大半(98.8%)が投与初期に発現しており、頻度は投与継続とともに低下する」と説明。感染症の予防とともに、抗サイトカイン療法やステロイド投与などCRSの管理が重要になるという。
以上を踏まえ、同氏は「エルラナタマブは臨床試験において良好な成績を示しており、MM患者の新たな治療選択肢となりうる」と述べた。また、実施施設や治療タイミングの点でCAR-T細胞療法に比べて制限が少ないことから、「利便性の高さも期待される」と説明した。
その上で、「今後は医療経済的な有益性の観点からも、エルラナタマブの早期使用によりMMの治癒を目指したい」と展望した。
(植松玲奈)